Zellfreie, azelluläre Matrixpräparate sind eine Option zur Deckung oberflächlicher Wunden. Wie dabei verfahren wird, lesen Sie hier in einem Beitrag von Dr. medic. Tania-Cristina Costea und PD Dr. rer. nat. Bernd Stratmann.
Chronische offene Wunden sind bei Patienten mit Diabetes mellitus eine häufige Folgekomplikation. Ergänzend zum physikalischen oder biologischen Debridement, um die avitale Wunde zu reaktivieren, werden feuchte Wundverbände eingesetzt, um optimale Granulationsbedingungen zu schaffen. Eine große Herausforderung ist die finale Deckung offener chronischer Läsionen. Nach operativem Eingriff steht nicht immer genügend Hautmaterial zur Verfügung, damit die Wunde verschlossen werden kann.
Oft fehlt bei großen oberflächlichen Läsionen das notwendige Granulationsgewebe für die Erneuerung und den Wundverschluss aus der Wunde heraus. Die Epithelialisierung kann nur unvollständig oder nicht konsequent vom Wundrand aus erfolgen, was letztlich zu Rezidiven mit dem Risiko für unvollständige Abheilung führt.
Basisgewebe für Zellproliferation und Zellmigration
Eine Option zur Deckung oberflächlicher Wunden neben allogener Spalthautpräparation sind zellfreie, azelluläre Matrixpräparate, mit denen das Behandlungsspektrum erweitert werden konnte. Als Spender für die Matrizen fungieren Rind oder Schwein (intestinale Mukosa) bzw. Amnion, in neuerer Zeit auch Fisch (Nordatlantik-Dorsch, Kabeljau).
Die Präparate dienen als Basisgewebe zur Zellproliferation (Weiterentwicklung) und Zellmigration (Einwanderung) durch darin enthaltene Zytokine (Botenstoffe) und Wachstumsfaktoren. Gleichzeitig wird das Entzündungsgeschehen (Inflammation) positiv beeinflusst und an der Wundheilung beteiligte Enzyme werden angeregt.
Förderung Gewebeneuaufbau und Angiogenese
Die marine Matrix enthält keine Hautzellen mehr, sie ist komplett dezellularisiert. Die Gewebestruktur wird als statisches Gerüst mit den darin enthaltenen Proteinen zur Verfügung gestellt. Verglichen mit Säugetiermatrizen kann die marine Matrix schonender hergestellt werden. Ihr antiinflammatorisches und antibakterielles Potential ist durch den Omega-3-Fettsäure-Gehalt deutlich höher.
Das marine Gewebe ähnelt im Aufbau der menschlichen Haut. Bei erhaltener Protein- und Matrixstruktur werden das Einwandern von Hautzellen und die Kapillarbildung erleichtert. Körpereigene Stammzellen wandern in das applizierte Gewebe ein, proliferieren dort, fördern den Gewebeneuaufbau und die Angiogenese. Zudem wird die Immunogenität (über z. B. Cytokin Interleukin -1ß) günstig beeinflusst.
Erste Effekte schon nach Erstapplikation
Die Omega-3-Wundmatrix ist als vakuumgetrocknetes Präparat in verschiedenen Größen erhältlich. Sie wird vor der Anwendung auf die Größe der Wundfläche zugeschnitten. Nach Anfeuchten der Matrix mit steriler physiologischer Kochsalzlösung (0,9%) wird die Wunde mit einem Schaumstoffverband abgedeckt. Der Verband wird unter Belassen des Omega-3-Xeno-Grafts alle zwei bis drei Tage gewechselt. Innerhalb von etwa sieben Tagen ist die Wundmatrix, die als Medizinprodukt zugelassen und CE-zertifiziert ist, nahezu vollständig resorbiert.
Oft zeigen sich positive Effekte schon nach Erstapplikation mit azellulärem Omega-3-Xeno-Graft. Die Behandlung gilt als abgeschlossen, sobald die Wunde verschlossen ist. Zusätzlich sind Druckentlastung und orthopädische Maßschuhe für den langfristigen Behandlungserfolg wichtig. Selbstredend ist die Optimierung der Stoffwechselparameter wichtiger Therapiebestandteil.
 Schematische Darstellung vom Gewinn der Matrix bis hin zur Applikation.
Schematische Darstellung vom Gewinn der Matrix bis hin zur Applikation.
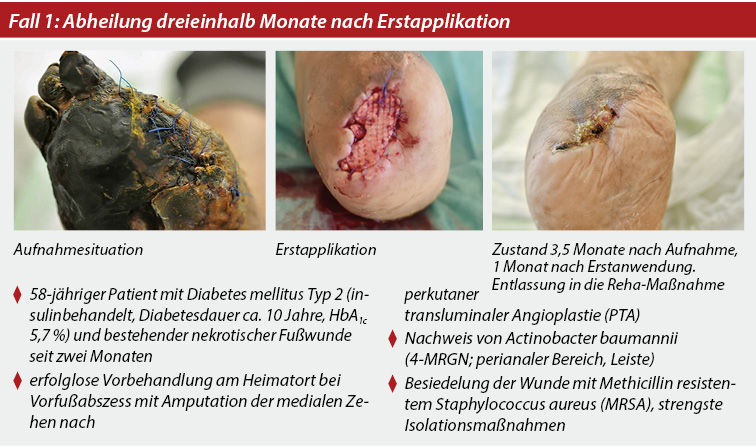
Im Folgenden werden drei Patientenbeispiele vorgestellt, die mit Omega-3-Wundmatrix behandelt wurden:
Der Patient wurde stationär mit gut demarkierter trockener Nekrose am rechten Vorfuß und Mittelfuß plantar mit distalem Knochenkontakt aufgenommen. Nach Antibiogramm wurde die bisherige antibiotische Therapie mit Clindamycin und Amoxicillin/Clavulansäure auf Fosfomycin und Cefuroxim umgestellt. Im ersten Schritt erfolgte eine Vorfußamputation (nach F. Chopart) mit im Verlauf rezidivierenden Fieberschüben und Ansteigen der Infektparameter bei infiziertem Hämatom an der Wunde und Auftreten nekrotischer Wundrandveränderung. Die Antibiose wurde um Imipinem erweitert und eine lokale VAC (Vacuum Assisted Closure)-Therapie über sieben Tage durchgeführt.
Nach erneuter Angiographie der rechten unteren Extremität wurde in der Mitte der Arteria femoralis superficialis (AFS) eine vorbestehende schwere, aber drahtgängige Dissektion mit deutlicher Flussbehinderung sowie eine weitere große nicht passierbare Dissektion am Übergang AFS/Arteria poplitea diagnostiziert, während in der proximalen AFS ein offenes Stentsegment vorhanden war. Im zweiten Schritt wurde eine digitale Substraktions-Angiographie (DSA) mit PTA und Stent-Implantation (antegrad transfemoral / retrograd transtibial) sowie eine lokales chemisches Debridement durchgeführt. Zur weiteren Wundbehandlung schlossen sich zwei Zyklen VAC-Therapie unter dualer Plättchen-Hemmung an.
Im Verlauf wurde zweimal der Fischhaut-basierte, azelluläre Xeno-Graft appliziert. Die Kontrolle zeigte eine deutliche Verkleinerung der Wunde mit zunehmender Epithelialisierung sowie nahezu vollständiger Abheilungstendenz. Nach Versorgung mit Interimsschuh wurde in der anschließenden Rehabilitationsmaßnahme eine vollständige Wundheilung innerhalb von zwei Monaten nach Erstapplikation der Omega-3-Wundmatrix erzielt.
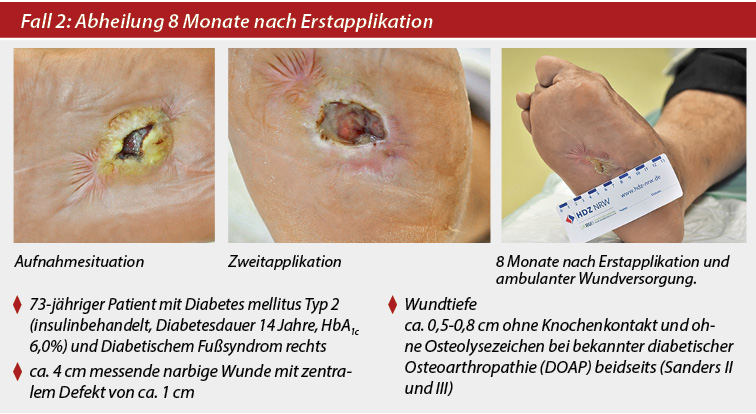
Nach Vorstellung des Patienten wurde rechtsseitig eine beginnende bis wenig ausgeprägte periphere arterielle Verschlusskrankheit (PAVK) diagnostiziert. Nach Katheteruntersuchung zeigte sich kein Befund einer Stenose von AFS/ Arteria poplitea/ Arteria tibialis anterior/ Arteria fibularis. Die Arteria tibialis posterior beim Patienten war eher schmalkalibrig angelegt mit bis zu 50%igen Stenosen ohne Interventionsbedarf.
Entsprechend dem Resistogramm wurde mit einer Ciprofloxacin-Therapie begonnen. Nach lokaler Unterdrucktherapie mit anschließender operativer Wundexzision wurden die Wundränder aufgefrischt. Es folgte erneut die Unterdrucktherapie. In der Folge wurde bei beginnender Ausbildung von Granulationsgewebe die Omega-3-Wundmatrix appliziert.
Die Kontrolle des Wundbefundes zeigte eine deutliche Verkleinerung der Wunde mit Nachweis zunehmender Epithelialisierung sowie Abheilungstendenz. Im Verlauf wurde das Verfahren wiederholt, was zu einen gutem Ergebnis bzgl. der Wundheilung führte. Der Patient wurde mit entsprechenden Maßschuhen versorgt und in die ambulante Weiterversorgung entlassen. Acht Monate nach Erstapplikation der Omega-3-Matrix konnte eine komplette Wundheilung erreicht werden.
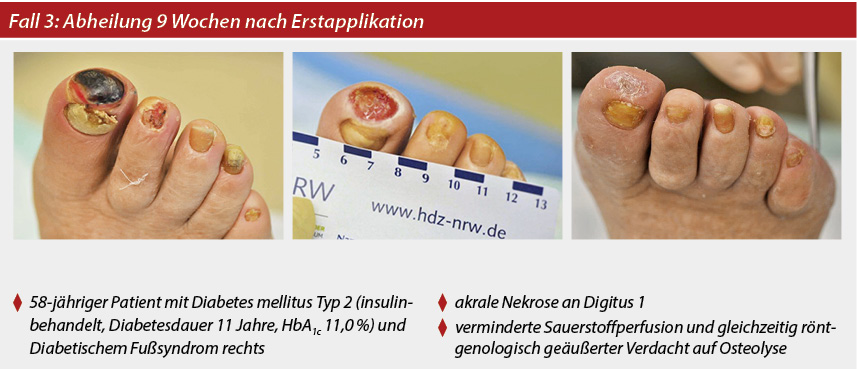
Nach stationärer Aufnahme des Patienten erfolgte im ersten Therapieschritt die stadiengerechte Wundbehandlung mit konsequenter Entlastung des Fußes inklusive chirurgischem Debridement (Nekrosektomie) und Antibiose nach Resistogramm. Zur Verbesserung der lokalen Durchblutung wurden täglich Infusionen mit Alprostadil durchgeführt.
Im Verlauf bei darstellbarem Knochenkontakt erfolgte eine zweimalige Wunddeckung mit Omega-3-Matrix im zweitägigen Abstand.
Bei Verlaufskontrolle des Wundbefundes zeigte sich eine gute Granulation der Wunde mit Nachweis zunehmender Epithelialisierung sowie Abheilungstendenz. Der Patient wurde mit entsprechendem Verbandsschuh versorgt und ambulant weiterbetreut. Eine komplette Wundheilung konnte neun Wochen nach Erstapplikation der Omega-3-Wundmatrix erzielt werden.
Schlussfolgerung
Bei gutem Durchblutungsstatus der unteren Extremität kann die Applikation von azellulärem Omega-3-Xeno-Graft zur beschleunigten Abheilung der Wunde führen. Die Behandlungsoption bietet somit ein zur allogenen Spalthautapplikation vergleichbares Resultat bei für den Patienten weniger invasivem Eingriff.
- Kein DFS darf ein Leben zerstören
- Management chronischer Wunden
- Einsatz von Kaltplasma in der Wundbehandlung
- Plastische Deckung chronischer Wunden
Erschienen in: Diabetes-Forum, 2018; 30 (4) Seite 20-22