Viele Diabetiker entwickeln im Laufe ihrer Erkrankung Wunden an den Füßen. Dr. Thomas Werner berichtet an dieser Stelle über eine neue Behandlungsmethode.
Viele Diabetiker entwickeln im Laufe ihrer Erkrankung Wunden an den Füßen. Eine entscheidende Rolle in der Genese des Diabetischen Fußsyndroms (DFS) spielen neben der fast immer nachweisbaren Polyneuropathie Perfusionsstörungen. Diese betreffen im Rahmen der Makroangiopathie die Arterien der Extremitäten (pAVK: periphere arterielle Verschlusskrankheit). Stenosen der Arterien können technisch meist bis weit in die Peripherie beseitigt werden. Mikrozirkulationsstörungen hingegen sind schlecht beeinflussbar und können in der Folge Wundheilungsstörungen begünstigen.
Zügiger Wundverschluss
Nicht selten sind chronische Verläufe, die auch unter regelmäßiger ärztlicher Behandlung und Entlastung der Wunde durch strenge Bettruhe oder technische Hilfsmittel (Filz, Orthopädietechnik etc.) kaum beeinflussbar sind. Häufig spielen zusätzlich Infektionen eine Rolle. Durch die gestörte Immunantwort bei Diabetes mellitus breiten sich bakterielle Erreger rasch aus. Sind die Wunden tief, kommt es zu Knocheninfektionen, die wiederum eine lange antibiotische Behandlungsdauer nach sich ziehen können.
Langzeitantibiosen oder bei Rezidiven die häufig wiederkehrende Antibiotikatherapie führen oft zur Resistenzentwicklung der Bakterien. Dies erschwert die Behandlung zusätzlich. Zur Wundbehandlung bei Menschen mit DFS sollten deshalb alle Möglichkeiten ausgeschöpft werden, einen zügigen Verschluss der Ulcera zu erreichen. Etabliert hat sich die V.A.C.-Pumpentherapie. Neu ist die Evidenz einer speziellen Wundauflage (Edmonds M et al.; Lancet 2017). Die hyperbare Sauerstofftherapie bleibt weiter umstritten und ist im Behandlungsalltag in der Regel nicht verfügbar.
Keine Wechselwirkungen von Kaltplasma mit Geweben
Ein neuer Therapieansatz zur Beeinflussung gleich mehrerer der oben beschriebenen Problemfelder zur Wundheilung bei DFS ist die Nutzung von medizinischem Plasma. Als Plasma bezeichnet man einen Aggregatszustand, den ein Gas erreicht, wenn man ihm Energie zuführt. In der Natur tritt dies beispielsweise bei Gewitterblitzen auf. Durch technische Neuerungen ist es mittlerweile möglich, das physikalische Phänomen medizinisch zu nutzen. Da keine hohen Temperaturen notwendig sind, bezeichnet man dies als kaltes Plasma. Was zunächst nach Science-Fiction klingt, ist durchaus anwenderfreundlich.
Durch den Einsatz elektrischer Energie kann Plasma in Form von Gasentladungen kontrolliert erzeugt werden. Kalte Plasmen gehen keine thermischen Wechselwirkungen mit Geweben ein. Die Wirkung auf Wunden kommt durch elektrische, photonische und chemische Energie zustande.
Bessere Wundheilung
In den Grundlagenstudien konnten mehrere Effekte nachgewiesen werden, die sich auch bei Wunden im Rahmen eines DFS positiv auswirken sollten. Wichtig ist die bewiesene Verbesserung der Mikrozirkulation. Außerdem wirkt Kaltplasma antimikrobiell, was unabhängig vom Erreger ist. Neben Pilzen sind besonders Bakterien interessant. Auch auf bestimmte Antibiotika nicht mehr ansprechende Keime wie Methicillin resistenter Staphylococcus aureus (MRSA) oder multiresistente, gramnegative Bakterien (MRGN) werden in der Wunde reduziert. Resistenzentwicklungen sind bisher nicht bekannt.
Sogar Biofilme sind durch Kaltplasma zu beeinflussen. Zur Förderung der Heilung tragen noch andere Effekte bei. So wird die Proliferation von Fibroblasten und Endothelzellen durch Stimulation von Fibroblast Growth Factor 2 (FGF-2) angeregt sowie die Zellmigration und Kollagensynthese verbessert.
Zur Beeinflussung der Wundheilung werden kurze Anwendungszeiten und geringe Dosen von Plasma eingesetzt. Dann sind positive Effekte zu beobachten. Bei hohen Plasmadosen und langer Anwendungszeit sind gegenteilige Wirkungen beschrieben (z.B. Zelltod durch Apoptose, Proliferationsstop, DNA-Schäden). Damit ergeben sich Chancen, das Verfahren zur Behandlung von Tumoren einzusetzen. Untersuchungen diesbezüglich sind bereits publiziert.
Ausgesuchte Studien
Eine Verbesserung der Mikrozirkulation durch Kaltplasma zeigt eine Arbeit von Kirsch T et al., in der die lokale Perfusion der Haut bei 20 gesunden Probanden untersucht wurde. Direkt nach der Anwendung von Plasma kam es zu einem um 73 % gesteigerten lokalen Blutfluss. Auch die bestimmte Sauerstoffsättigung im Gewebe war signifikant erhöht.
Die Wirkung von medizinischem Plasma auf Bakterien zeigt sehr plastisch eine Publikation von Dezest M et al. aus dem Jahr 2017. Hier wurden neben den statistischen Untersuchungen mikroskopische Bilder von Escherichia coli (E. coli) vor und nach Anwendung des Verfahrens dargestellt. Recht deutlich zu erkennen ist die zerstörte Oberfläche der Bakterien nach Behandlung (Abb. 2).
Brehmer F et al. publizierten 2014 eine randomisierte Studie über die Wirkung von Kaltplasma auf die bakterielle Kolonisation von venösen Ulcera. 14 Patienten wurden standardisiert lokal behandelt. Bei der Hälfe der Patienten kam zusätzlich Kaltplasma zur Anwendung. Mittels vor und nach Plasmabehandlung aufgelegter Agarplatten wurde die bakterielle Besiedlung der Wunden in beiden Gruppen kontrolliert. Außerdem wurde die Entwicklung der Ulcusgröße dokumentiert. Hier zeigten sich Vorteile im Therapiearm.
Geräte zur Anwendung von Kaltplasma
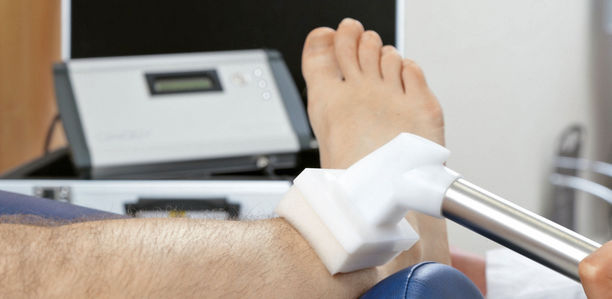
In Deutschland sind mehrere Geräte zur Kaltplasmatherapie erhältlich. Das Plasma wird technisch strahlförmig oder flächig freigesetzt. Die Applikation erfolgt entweder über eine Art Stift (kINPen® MED; neoplas tools GmbH Greifswald/ Abb. 1a und Abb. 1b) oder über einen schwammartigen Spacer (PlasmaDerm®; CINOGY Duderstadt/ Abb. 1c und Abb. 1d). Berichtet wird auch über neu entwickelte Silikon-Wundauflagen (Plasma-Patches; COLDPLASMATECH GmbH Greifswald und CINOGY Duderstadt). Diese sind allerdings derzeit noch nicht erhältlich.
Die Firma plasma MEDICAL SYSTEMS® GmbH in Nievern bietet ein kleines transportables, akkubetriebenes Gerät (plasma ONE®) zur Kaltplasmatherapie an. Das System arbeitet ebenfalls mit einem stiftförmigen Applikatorsystem. Adtec Plasma Technology aus Großbritannien verfügt über eine Apparatur namens Adtec SteriPlas®.
Während der kiNPen® und der SteriPlas® Argongas zur Erzeugung des Plasmas benötigt, reicht für die beiden anderen Systeme Raumluft. Neben der Behandlung chronischer Wunden werden unterschiedliche Anwendungsgebiete beworben, zum Beispiel die Zahnmedizin oder Dermatologie. Allen gemeinsam ist die einfache und nebenwirkungsarme Art der Anwendung.
- Kein DFS darf ein Leben zerstören
- Management chronischer Wunden
- Einsatz von Kaltplasma in der Wundbehandlung
- Plastische Deckung chronischer Wunden
Erschienen in: Diabetes-Forum, 2018; 30 (4) Seite 18-19