Eine neue Studie liefert erstmals detaillierte Einblicke in die mikroskopischen Veränderungen der Bauchspeicheldrüse bei Typ‑2‑Diabetes. Möglich wird dies durch erklärbare Künstliche Intelligenz (KI), die zeigt, welche Gewebestrukturen für die Diagnose relevant sind und wie sich das zelluläre Umfeld der Langerhans‑Inseln bei der Erkrankung verändert.
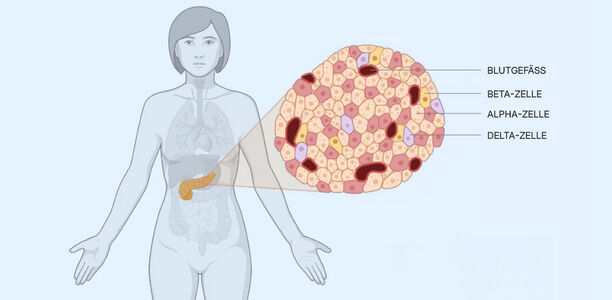
Typ‑2‑Diabetes zählt zu den weltweit häufigsten chronischen Erkrankungen und wird meist anhand erhöhter Blutglukosewerte diagnostiziert. Diese Parameter bilden jedoch vor allem die Folgen der Erkrankung ab. Die wesentlichen Veränderungen entstehen im Pankreas, insbesondere in den Langerhans‑Inseln, in denen Beta‑, Alpha‑ und Delta‑Zellen gemeinsam die Glukosehomöostase steuern. Zusätzlich wirken Blutgefäße, Bindegewebe, Fettzellen und Nervenfasern auf dieses fein regulierte Netzwerk ein. Wie sich dieses Zusammenspiel bei Typ‑2‑Diabetes strukturell verändert, war bislang nur schwer erfassbar, da individuelle Unterschiede im Gewebe eine visuelle Beurteilung erschweren.
KI‑gestützte Analyse identifiziert relevante Muster
Forschende des Deutschen Diabetes‑Zentrums (DDZ), des Paul Langerhans Instituts am Universitätsklinikum Dresden, des Instituts für Diabetesforschung und Metabolische Erkrankungen in Tübingen sowie weiterer Partnerinstitutionen nutzten KI, um neue Einblicke in diese Prozesse zu gewinnen.
„Mit 100 Proben aus Dresden und Tübingen haben wir einen der bislang umfangreichsten Datensätze aus Gewebeabschnitten der Bauchspeicheldrüse aufgebaut“, erläutert Dr. Felicia Gerst. Die Proben stammten von Personen, die sich aus unterschiedlichen medizinischen Gründen einer Pankreasoperation unterzogen hatten.
Auf Basis dieser Gewebeschnitte trainierte das Team ein Modell des maschinellen Lernens, das zwischen Proben von Menschen mit und ohne Typ‑2‑Diabetes mit hoher Genauigkeit unterscheiden kann. Besonderer Wert wurde auf Erklärbarkeit gelegt: Das System markiert jene Bereiche im Bild, die für die Entscheidung maßgeblich waren. Diese Hervorhebungen lassen sich anschließend biologisch interpretieren und statistisch validieren.
Veränderungen betreffen das gesamte Inselgewebe
Die Auswertungen zeigen, dass nicht nur Beta‑Zellen betroffen sind. Auch Alpha‑ und Delta‑Zellen weisen bei Typ‑2‑Diabetes veränderte Positionierungen und Verteilungen auf. Zudem sind die Langerhans‑Inseln insgesamt kleiner. Eine weitere Beobachtung betrifft Fettzellen im unmittelbaren Umfeld der Inseln, die bei Betroffenen deutlich häufiger auftreten.
„Diese Nähe könnte die Funktion der hormonproduzierenden Langerhans‑Inseln beeinflussen“, erklärt Professor Robert Wagner vom Deutschen Diabetes‑Zentrum. Die Ergebnisse liefern aus seiner Sicht wichtige Ansatzpunkte für künftige Untersuchungen. Wagner betont, dass ein besseres Verständnis der strukturellen Krankheitsmechanismen die Entwicklung gezielter therapeutischer Strategien erleichtern könne.
Auch Dr. Michele Solimena, Professor für Molekulare Diabetologie am Universitätsklinikum Dresden, unterstreicht den integrativen Ansatz: „Das Forschungsprojekt zeigt, dass wir nicht nur einzelne Zellen, sondern das gesamte mikroskopische Netzwerk der Bauchspeicheldrüse betrachten müssen, um Diabetes besser zu verstehen.“ Das Forschungsteam stellt zudem den vollständigen Code für Bildvorverarbeitung, Modelltraining und Analyse offen zur Verfügung, um Transparenz herzustellen und weiteren Projekten den methodischen Zugang zu erleichtern.
von Redaktion diabetologie-online
mit Materialien des Deutschen Diabetes‑Zentrums (DDZ)