Aktualisierte Stellungnahme der DDG-Arbeitsgemeinschaft Diabetes & Technologie (AGDT) zum Ersatz von Blutglukosemessungen durch Messungen mit Systemen zum kontinuierlichen real-time-Glukosemonitoring (rtCGM) oder mit intermittierendem Scannen (iscCGM).
Revidierte Version vom 28. Mai 2019.
Systeme zum kontinuierlichen Glukosemonitoring (CGM) liefern Menschen mit Diabetes wesentlich umfassendere Informationen über ihre aktuelle Glukosesituation als punktuelle konventionelle kapilläre Blutglukosemessungen. CGM-Systeme messen den Glukosegehalt in der interstitiellen Flüssigkeit des Unterhautfettgewebes. Als real-time-CGM (rtCGM) werden laut Beschluss des Gemeinsamen Bundesausschusses (G-BA) im Jahr 2016 Systeme bezeichnet, die automatisch Messwerte an ein Empfangsgerät übertragen, kontinuierlich Messwerte und Trends zum Glukosegehalt anzeigen sowie individuell einstellbare Alarmfunktionen besitzen.
Zusätzlich zu den rtCGM-Systemen sind iscCGM-Systeme verfügbar. Diese Systeme zum intermittierenden Scannen eines CGM-Sensors (iscCGM) werden vom Hersteller als Flash-Glukosemonitoring (FGM) bezeichnet. IscCGM-Systeme unterscheiden sich von rtCGM-Systemen durch die Notwendigkeit eines Scanvorgangs zum Generieren eines Messwerts. Es erfolgt keine kontinuierliche automatische Übertragung der Glukosewerte an ein Empfangsgerät. Die neueste Generation der iscCGM-Systeme bietet Alarmfunktionen wie Hoch- und Tiefalarm auch in der Zeit zwischen den Scans. Allerdings muss bei diesen Systemen nach einer Alarmierung weiterhin ein Scanvorgang zur Anzeige des Messwerts erfolgen.
Ziel dieser Stellungnahme ist es, den aktuellen wissenschaftlichen Stand für die Nutzung von rtCGM-/iscCGM-Systemen als Ersatz für Blutglukosemessungen darzustellen, d. h. Systeme mit einem "Replacement Claim" (s. u.). Allgemeine Hinweise zur Glukosemessung können der aktuellen Praxisempfehlung "Glukosemessung und -kontrolle bei Typ-1- oder Typ-2-Diabetes" der Deutschen Diabetes Gesellschaft (DDG) entnommen werden [Heinemann 2018a]. Praktische Tipps der AGDT zum Einsatz von rtCGM und iscCGM stehen als Ergänzung zu dieser Stellungnahme in der Anlage 1.
1. Aktueller Stand
Glukosedaten der rtCGM-Systeme Dexcom G5 und G6 des Unternehmens Dexcom sowie der iscCGM-Systeme FreeStyle Libre und FreeStyle Libre 2 des Unternehmens Abbott können laut jeweiliger Bedienungsanleitung für Therapieentscheidungen verwendet werden (Tab. 1). Dieses wird auch "non-adjunctive usage" oder "Replacement Claim" genannt. Therapieentscheidungen beziehen sich insbesondere auf die Festlegung und Berechnung der Insulindosierung und basieren auf den Gewebeglukosewerten.
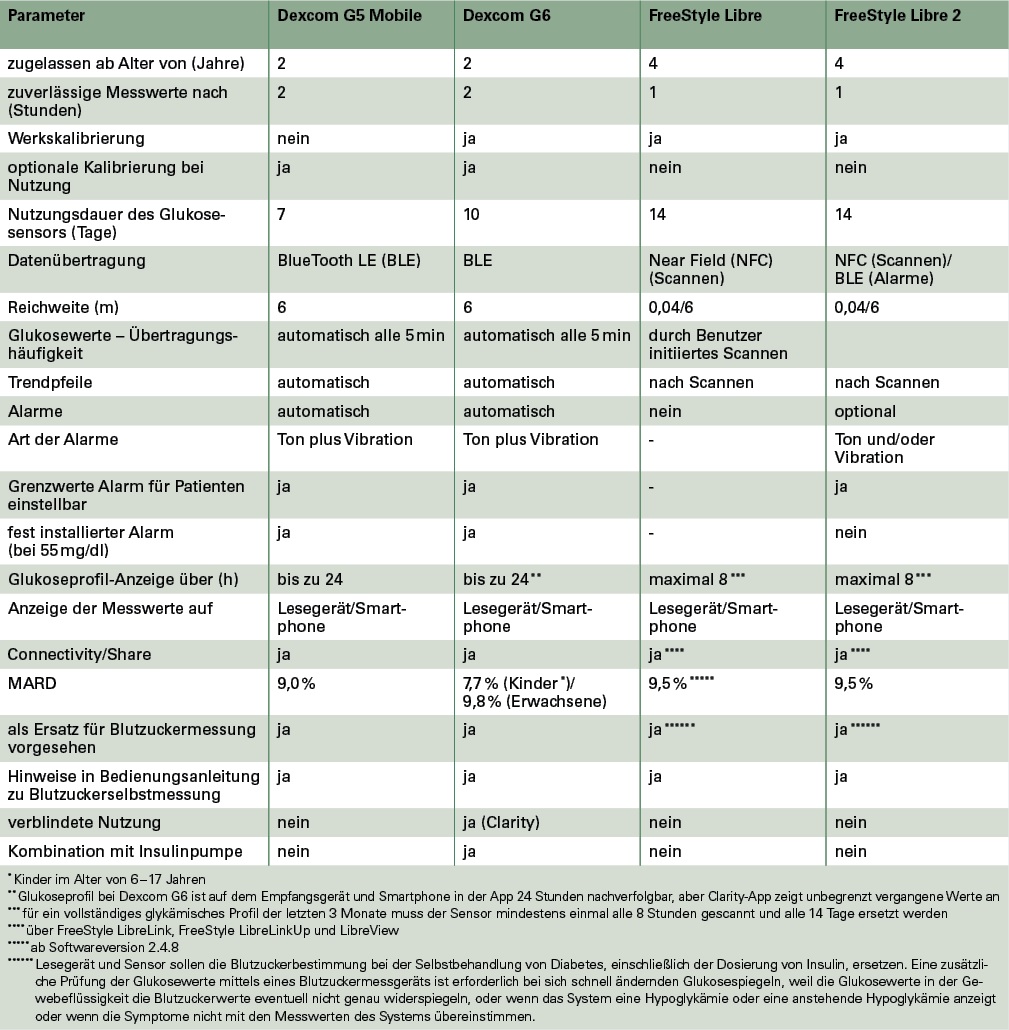 Tab. 1: Vergleich der Eigenschaften zweier rtCGM-System-Generationen (Dexcom G5 Mobile und Dexcom G6 von Dexcom) und der beiden Generationen eines iscCGM-Systems (FreeStyle Libre und FreeStyle Libre 2 von Abbott).
Tab. 1: Vergleich der Eigenschaften zweier rtCGM-System-Generationen (Dexcom G5 Mobile und Dexcom G6 von Dexcom) und der beiden Generationen eines iscCGM-Systems (FreeStyle Libre und FreeStyle Libre 2 von Abbott).
In den Bedienungsanleitungen werden dennoch ausdrücklich Situationen benannt, in denen zusätzlich der Blutglukosewert bestimmt werden soll (diese werden hier nicht weiter aufgelistet, bitte bei den jeweiligen Herstellern nachsehen). Die Nutzer sollten über die Limitationen der CGM-Systeme, über die Ausnahmefälle, die eine Blutglukoseselbstmessung laut Bedienungsanleitung erforderlich machen, sowie über mögliche Interferenzen mit Medikamenten (z. B. Paracetamol) oder anderen Substanzen (z. B. Vitamin C) informiert sein. Auch Hinweise der Hersteller hinsichtlich der Altersgruppen der Nutzer in den Bedienungsanleitungen sind zu beachten. Bei weiteren verfügbaren rtCGM-Systemen, wie Guardian (Medtronic) und Eversense (Roche/Senseonics) müssen laut Herstellerangaben noch Blutglukosemessungen bei Therapieentscheidungen durchgeführt werden. In diesem Artikel werden wir uns ausschließlich auf die CGM-Systeme beziehen, die als Ersatz für Blutglukosemessungen zugelassen sind.
Ein weiteres wichtiges Thema bei der Nutzung von rtCGM-Systemen ist die Kalibration. Aktuell ist nur das Dexcom-G5-Mobile-System regelmäßig 2 × täglich zu kalibrieren. Bei dem Nachfolgemodell Dexcom G6 ist die Kalibration optional, d. h. das Dexcom-G6-System ist werkskalibriert, kann aber bei Bedarf durch den Anwender zusätzlich kalibriert werden. Die iscCGM-Systeme FreeStyle Libre und FreeStyle Libre 2 sind werkskalibriert ohne die Möglichkeit einer individuellen Nachkalibration durch den Nutzer.
2. Messgenauigkeit
Herstellerangaben Dexcom G5 Mobile
Laut der Bedienungsanleitung des Dexcom G5 Mobile wiesen bei Glukosekonzentrationen von 80 mg/dl oder weniger bei Erwachsenen 93 % der Messwerte eine Abweichung unter ± 20 mg/dl auf. Bei Werten über 80 mg/dl betrug die Abweichung bei 93 % der Messwerte weniger als ± 20 % im Vergleich zu den mit einer Labormethode in Blutproben gemessenen Werten. 99 % der Messwerte lagen innerhalb von ± 40 mg/dl Abweichung bei Glukosekonzentrationen von 80 mg/dl oder weniger bzw. 40 % Abweichung bei Glukosekonzentrationen über 80 mg/dl. Bei Kindern wiesen 91 % der Messwerte eine Abweichung unter ± 20 mg/dl bei Glukosekonzentrationen unter 80 mg/dl auf. Bei Werten über 80 mg/dl lagen die Abweichungen bei Werten unter ± 20 %. 98 % der Messwerte lagen innerhalb von ± 40 mg/dl bzw. ± 40 % Abweichung.
Herstellerangaben Dexcom G6
Laut der Gebrauchsanweisung des Dexcom G6 lagen 92 % der Messwerte bei Erwachsenen innerhalb der Zone A der Clarke-Error-Grid-Darstellung sowie 100 % der Messwerte innerhalb der Zonen A und B. Bei pädiatrischen Patienten lagen 96 % der Messwerte innerhalb der Zone A sowie 99,8 % der Messwerte innerhalb der Zonen A und B. Bei Erwachsenen liegt die "Mean Absolute Relative Difference" (MARD) bei 9,8 % über den gesamten Tragezeitraum von 10 Tagen in einem Glukosemessbereich von 40 bis 400 mg/dl. Als Referenz wurde ein YSI-Laboranalysator eingesetzt. Bei Kindern liegt die MARD für den gesamten Tragezeitraum bei 7,7 %.
Herstellerangaben FreeStyle Libre
Laut Angaben des Herstellers auf seiner Homepage lagen 86,7 % der Messwerte bei Erwachsenen innerhalb der Zone A der Clarke-Error-Grid-Darstellung sowie 99,7 % der Messwerte innerhalb der Zonen A und B. Die MARD im Vergleich zur Blutzuckerselbstmessung beträgt 11,4 % über den gesamten Tragezeitraum von 14 Tagen.
Herstellerangaben FreeStyle Libre 2
Laut Herstellerangaben auf der Homepage wiesen 90,3 % der Messwerte bei Glukosekonzentrationen unter 80 mg/dl bzw. ≥ 80 mg/dl eine Abweichung von weniger als ± 20 mg/dl bzw. ± 20 % auf. Es lagen 89 % der Messwerte innerhalb der Zone A der Clarke-Error-Grid-Darstellung sowie 100 % der Messwerte innerhalb der Zonen A und B. Die MARD im Vergleich zur Blutzuckerselbstmessung beträgt 9,5 % über den gesamten Tragezeitraum von 14 Tagen.
Der FreeStyle Libre 2 zeigt bei Erwachsenen eine über 14 Tage ermittelte verbesserte MARD von 9,5 %. Die MARD am ersten Tag konnte auf 10,9 % reduziert werden und an Tag 6 wurden 8,8 %, an Tag 11 9,3 % und an Tag 14 9,0 % erreicht (Fact Sheet Messgenauigkeit). Die Ergebnisse des pädiatrischen Teils der Genauigkeitsdaten zum FreeStyle Libre 2 wurden auch verbessert. Die MARD über 14 Tage liegt bei 9,4 %. Die Verbesserung am ersten Tag bei der MARD bildet sich mit 11,3 % ab und in den 13 Folgetagen stabilisiert sie sich zwischen 8,2 und 9,5 %.
Insgesamt gilt es zu beachten, dass die Genauigkeitsangaben der verschiedenen CGM-Systeme nicht unter identischen Bedingungen erfasst wurden, d. h. ein Vergleich ist nur eingeschränkt möglich.
3. Studienergebnisse zur Messgenauigkeit
Messgenauigkeit von Blutzuckermesssystemen
Bei Blutglukosemesssystemen gibt es die ISO-Norm 15197:2013, die u. a. Vorgaben zur Ermittlung der Messgenauigkeit und der Akzeptanzgrenzen macht. Hiernach ist eine maximale Abweichung unter ± 15 mg/dl bzw. gleich ± 15 % bei Glukosekonzentrationen unter 100 mg/dl bzw. gleich oder über 100 mg/dl für 95 % der Ergebnisse erforderlich.
Eine verbindliche Vorgabe im Sinne eines zu erfüllenden Standards bei der analytischen Messgüte gibt es bisher weder für die rtCGM-Systeme noch für die iscCGM-Systeme (siehe 8.). Häufig wird die MARD (Mean Absolute Relative Difference) als Parameter für die Genauigkeit angegeben. Allerdings weist die MARD als Genauigkeitsparameter verschiedene Schwächen auf [Reiterer 2017], daher sind nur durch "Head-to-Head"-Studien verschiedene Systeme gut vergleichbar.
4. Messgenauigkeit und "Replacement"
Kovatchev und Kollegen haben durch Modellberechnungen eine Mindestgenauigkeit von unter oder gleich 10 % bei der MARD ermittelt, bei der Entscheidungen zur Insulindosierung anhand von rtCGM-Werten mit ausreichender Sicherheit möglich sind [Kovatchev 2015]. Gleichzeitig wiesen sie auf eine zusätzliche deutliche Senkung der mittleren Glukosewerte und eine weitere Vermeidung von Hypoglykämien bei der Verwendung von Schwellen- und prädiktiven Alarmen hin.
In der Studie von Bailey et al. mit dem bisherigen iscCGM-System wies nur ca. die Hälfte der Sensoren eine MARD auf, die nach den erwähnten Modellberechnungen für eine Festlegung der Insulindosis empfehlenswert ist [Bailey 2015]. Weiterhin war die beobachtete Messgenauigkeit des iscCGM-Systems am ersten Tag der Nutzung, d. h. am Tag des Legens des Sensors, mit mittleren MARD-Werten von ~ 15 % weniger gut als an den folgenden 13 Tagen der Nutzungsdauer mit im Mittel 11 %. Diese Ergebnisse in Verbindung mit der Aussage zum Ersatz von SMBG wurden in der Literatur diskutiert [Bailey 2016, Freckmann 2016]. Leider werden nicht von allen Herstellern Angaben zu den MARD-Werten am ersten Tag angegeben.
Bei den rtCGM-Systemen und den iscCGM-Systemen gibt es eine "Run-in"-Phase mit teilweise deutlichen Abweichungen zur Blutglukose in der Zeit unmittelbar nach dem Legen des Sensors. Wie viele Studien zeigen, führt dies zu einer höheren MARD am ersten Tag nach dem Setzen, an den Nachfolgetagen ist die MARD üblicherweise besser.
Aktuelle Systeme
In der Zulassungsstudie von Wadwa et al. mit dem rtCGM-System Dexcom G6 unter Studienbedingungen (d. h. in der Klinik bei drei Messreihen mit Kohlenhydrat- und Insulinzufuhr, um den gesamten Glukosebereich von 40 bis 400 mg/dl abzudecken; zudem wurde nicht der nun verfügbare Applikator benutzt) lag die MARD bei Erwachsenen (n = 134) bei 9,9 %, bei Kindern und Jugendlichen (n = 128) bei 10,1 % und insgesamt bei 10 %. Nach 10 Tagen funktionierten noch 87 % der Sensoren [Wadwa 2018]. In der klinischen Studie von Shah et al. [Shah 2018] mit dem rtCGM-System Dexcom G6 (mit dem zugehörigen Applikator zum Setzen des Sensors und ohne studienbedingte Manipulationen bei den Glukosekonzentrationen) lag die MARD bei Erwachsenen bei 9,8 %, bei Kindern und Jugendlichen bei 7,7 % und insgesamt bei 9,0 %. In der Untersuchung von Welsh et al. mit Kindern und Jugendlichen (n = 37) lag die Gesamt-MARD bei 7,7 %, am ersten Tag bei 10,5 % und in den Folgetagen zwischen 6,2 % und 7,8 % [Welsh 2019]. Eine gewisse "Drift", die zur Verschlechterung der Messgüte der Glukosesensoren über die Tragedauer hinweg führen kann, kann bei Dexcom-G6-Systemen durch Kalibration kompensiert werden. Dabei muss die Kalibration korrekt durchgeführt werden; es liegen nur wenige Daten vor, die zeigen, wie gut dies in der Praxis erfolgt.
Head-to-Head-Studien
In den letzten Jahren sind mehrere Studien zur Untersuchung der Messgenauigkeit verschiedener CGM-Systeme publiziert worden. Boscari et al. haben in einer 2018 publizierten Studie gezeigt, dass sich unter Verwendung von Kapillarblutglukosewerten als Referenz für Dexcom G5 Mobile MARD-Werte von 9,8 % und für FreeStyle Libre eine MARD von 12,3 % ergaben [Boscari 2018]. Die Verwendung von venösen Blutproben mit einer Laborreferenz ergab MARD-Werte von 10,7 % bzw. 14,7 %.
In einer Studie von Freckmann et al., die ebenfalls 2018 publiziert wurde, erfolgte die Auswertung der Daten unter der Berücksichtigung der Patientenperspektive: Für das Dexcom G5 Mobile wurde der letzte innerhalb von 5 Minuten angezeigte Wert verwendet, für das FreeStyle Libre die Scan-Werte. Hier lag die MARD unter Verwendung von Kapillarblutglukosewerten bei 12,4 % für Dexcom G5 Mobile bzw. 13,0 % für FreeStyle Libre [Freckmann 2018]. Während Phasen induzierter starker Glukoseschwankungen lag die MARD gegenüber einer venösen Laborreferenz bei 16,2 % bzw. 16,8 %.
5. Studiengrundlagen für den Replacement-Claim
Für das rtCGM-System Dexcom G5 Mobile wurde 2017 durch Aleppo et al. in der REPLACE-BG-Studie gezeigt, dass die Nutzung ohne zusätzliche Blutzuckermessungen (d. h. Messungen, die über die für die Kalibration benötigten Messungen hinausgehen) sicher und effizient ist [Aleppo 2017]. Diese Ergebnisse dienten zusammen mit Studiendaten unter Verwendung des Dexcom-G4-Platinum-Systems mit Software 505, des Dexcom G6 in Human-Factors-Untersuchungen sowie in In-silico-Simulationen als Grundlage für die Erteilung des Replacement-Claims durch die Food and Drug Administration (FDA). In der klinischen Anwendung zeigten die Ergebnisse der randomisierten und kontrollierten DIAMOND-, GOLD- und HypoDE-Studien eine Reduktion entweder des HbA1c-Werts oder der Anzahl oder Dauer von Hypoglykämien bei gleichzeitiger Verringerung der Anzahl an Blutglukosemessungen [Beck 2017, Heinemann 2018b, Lind 2017].
Bei dem iscCGM-System liegen die Ergebnisse von zwei randomisierten, kontrollierten klinischen Studien (hoher Evidenzgrad) mit Patienten mit Typ-2-Diabetes (REPLACE-Studie) und mit Typ-1-Diabetes (IMPACT-Studie) vor [Bolinder 2016, Haak 2017]. Dabei wurde bei der REPLACE-Studie das primäre Studienziel, eine Reduktion des HbA1c-Werts, nicht erreicht. Allerdings wurde die Zeit im hypoglykämischen Bereich gesenkt. In der IMPACT-Studie wurde durch den Einsatz des iscCGM-Systems die Zeit im hypoglykämischen Bereich reduziert, ohne einen Anstieg des HbA1c-Werts nach sich zu ziehen, aber auch keine Verbesserung. Bei allen Studien haben die Patienten ihre Insulindosis aufgrund der Glukosemesswerte des rtCGM-/iscCGM-Systems angepasst.
In der IMPACT-Studie haben die Patienten bis zu 15-mal pro Tag ihre Glukosewerte mit dem iscCGM-System erfasst, aber nur noch 0,5-mal pro Tag konventionell ihren Blutglukosewert bestimmt [Bolinder 2016]. Die publizierten Daten liefern keinen Hinweis darauf, dass die genannten Tage/Situationen mit höheren MARD-Werten eine sicherheitsrelevante Auswirkung haben. Die Frage ist, ob und wie sich Studienbedingungen auf die Anwendung unter Alltagsbedingungen übertragen lassen.
In der IMPACT- und der REPLACE-Studie wurde zum Studienstart deutlich mehr Zeit im hypoglykämischen Bereich beobachtet, allerdings jeweils gemessen anhand der iscCGM-Werte und nicht kontrolliert durch SMBG wie in anderen CGM-Studien. Ausgehend von einer möglichen negativen systematischen Messabweichung, d. h. häufigen falsch niedrigen Werten beim iscCGM-System, sollten vor allem im niedrigen Wertebereich vergleichende Blutglukosemessungen erfolgen. Es stellt sich auch die Frage, wie zuverlässig Studienergebnisse sind, die sich ausschließlich auf iscCGM-Daten und nicht auf Blutglukosedaten als Kontrollen stützen [Pleus 2018].
Nebenwirkungen
Schwerwiegende produktbezogene unerwünschte Ereignisse wie schwere produktbezogene Hypoglykämien traten in der REPLACE-Studie nicht auf. Bei 6 Teilnehmern wurden insgesamt 9 produktbezogene unerwünschte Ereignisse dokumentiert, die allesamt als Reaktionen auf das Sensorpflaster kategorisiert wurden [Haak 2017].
In der IMPACT-Studie wurden keine produktbezogenen Hypoglykämien oder schwerwiegenden unerwünschten Ereignisse berichtet [Bolinder 2016]. Die 13 produktbezogenen unerwünschten Ereignisse waren lokale Hautreaktionen an der Sensorinsertionsstelle, davon wurden 6 als schwer beschrieben.
In der REPLACE-BG-Studie traten keine schwerwiegenden Hypoglykämien oder schwerwiegenden unerwünschten Ereignisse mit Produktbezug auf. Über nicht schwerwiegende unerwünschte Ereignisse wurde nicht berichtet [Aleppo 2017].
6. Notwendigkeit von Schulung
Für einen adäquaten, d. h. effizienten und sicheren, Ersatz von SMBG durch rtCGM-/iscCGM-Messungen sind eine technische Einweisung der Anwender sowie eine hohe analytische Messgenauigkeit der Systeme erste Voraussetzung. Für Menschen mit Diabetes, die bisher ihre Therapieentscheidungen auf präprandiale Blutglukosemessungen gestützt haben, stellt die Menge an Informationen, die rtCGM-Systeme oder iscCGM-Systeme zur Verfügung stellen, eine Herausforderung dar. Daher muss eine Schulung zur Nutzung der Daten durchgeführt werden, die den Anwender in die Lage versetzt, die komplexen Informationen der CGM-Systeme sicher in Therapieentscheidungen umzuwandeln. Hierzu wurden die Schulungsproramme Spectrum (rtCGM) und Flash (iscCGM) entwickelt.
Wichtig ist es auch, Anwender auf die Limitationen der Systeme hinzuweisen wie die druckinduzierte Sensorabschwächung [Baysal 2014]. Bei manchen rtCGM-Systemen (z. B. Dexcom G5 Mobile) ist eine ausgeprägte Erhöhung der Messwerte bei Einnahme von paracetamolhaltigen Medikamenten zu beobachten (aber nicht mehr beim Dexcom-G6-System) [Maahs 2015], bei dem iscCGM-System können laut Packungsbeilage Substanzen wie Ascorbinsäure und Salizylsäure die Messung beeinflussen. Auch gilt es, Anwender auf produktspezifische Besonderheiten hinzuweisen. So gibt es z. B. bei dem Dexcom-G5-Mobile-System eine optische Warnung (3 Fragezeichen) beim Auftreten eines temporären Sensorproblems, welches die Genauigkeit der gemessenen Werte betrifft und bei dem erst nach 3 Stunden ein akustischer Alarm ausgelöst wird (beim Dexcom G6 löst dieser Zustand die Warnung "Keine Messwerte" aus). Weiterhin gibt es Unterschiede zwischen den CGM-Systemen zu beachten. Bei rtCGM-Systemen erfolgt eine regelmäßige automatische Übertragung und Anzeige der Werte an ein Empfangsgerät, bei iscCGM-Systemen werden die Werte erst nach dem Scannen des Sensors angezeigt. Bei der zweiten Generation des iscCGM-Systems gibt es nun die Möglichkeit für den Patienten, bestimmte Schwellenwert-Alarme hinzuzuschalten. Es bleibt aber die Notwendigkeit des Scannens, um die aktuellen Messwerte zu erhalten. Entsprechend den Herstellervorgaben sollte unter Umständen eine Bestätigung der angezeigten Werte durch eine Blutglukosemessung erfolgen (s. u.).
Es ist wichtig, allen Anwendern zu vermitteln, dass rtCGM-/iscCGM-Systeme die Glukosekonzentration in der interstitiellen Flüssigkeit und nicht direkt im Blut bestimmen. Insbesondere in Phasen mit schnellen Glukoseänderungen in einem der beiden Kompartimente können erhebliche Abweichungen der Messwerte im Vergleich zum anderen Kompartiment auftreten [Siegmund 2017]. Dabei repräsentieren solche Abweichungen nicht unbedingt Messfehler, sondern haben physiologische Ursachen.
In Deutschland ist für rtCGM-Systeme ein herstellerunabhängiges und produktneutrales Schulungsprogramm verfügbar (SPECTRUM) [Gehr 2017]. Aktuell läuft eine Evaluierungsstudie für Spectrum (CGM-TRAIN-Studie). Für das iscCGM-System gibt es ebenfalls ein Schulungsprogramm (flash), welches vom Hersteller dieses Systems initiiert wurde. Die Ergebnisse der Evaluierungsstudie für das Schulungsprogramm Flash wurden kürzlich publiziert [Hermanns 2019].
7. Wichtig bei Therapieanpassungen
Aufgrund der bereits genannten spezifischen Unterschiede und basierend auf den Herstellerhinweisen in den jeweiligen Handbüchern sollten die Anwender bei Therapieentscheidungen eine gewisse Vorsicht walten lassen. Die Anwender sollten den Messergebnissen der CGM-Systeme nicht "blind" vertrauen und für eine Übergangsphase Blutzucker-Parallelmessungen bei Therapieentscheidungen durchführen. Dies gilt insbesondere während der ersten 24 Stunden eines neu angelegten Sensors. Dieses Vorgehen hilft, die neuen diagnostischen Möglichkeiten so sicher wie möglich zu nutzen, aber auch die Grenzen dieser Systeme zu erkennen und Risiken vorzubeugen.
Gleichzeitig sollten die Patienten entsprechend den Herstellervorgaben wissen, wann eine zusätzliche Blutglukosemessung erforderlich ist, um eine Therapieentscheidung zu treffen. Bei den Dexcom-rtCGM-Systemen ist dies beispielsweise der Fall, wenn die Symptome nicht mit den angezeigten Werten übereinstimmen und wenn entweder kein Glukosewert oder kein Trendpfeil angezeigt wird. Bei dem iscCGM-System sollte die Blutglukosemessung im Fall einer Hypoglykämie (< 3,9 mmol/l bzw. < 70 mg/dl), bei einer drohenden Hypoglykämie, bei schnell wechselnden Gewebeglukosewerten und bei Symptomen einer Hyper- oder Hypoglykämie durchgeführt werden.
8. Vorschlag der amerikanischen Gesundheitsbehörde für einen Standard bei CGM-Systemen
Im Zusammenhang mit dem Replacement von Blutglukosemessungen durch CGM-Systeme ist es wichtig, klarzustellen, dass bisher keine weltweit verbindlichen klinischen oder technischen Mindeststandards für rtCGM-/iscCGM-Systeme definiert wurden. Im März 2018 hat das Center for Devices and Radiological Health (CDRH) der amerikanischen Gesundheitsbehörde (FDA) Empfehlungen herausgegeben, welche Kriterien für die Zulassung von kontinuierlichen Messsystemen als "integriertes CGM" (iCGM) enthalten [U. S. Food and Drug Administration 2018]. Diese iCGM-Messsysteme müssen nicht nur Anforderungen hinsichtlich der Kommunikation mit anderen therapeutischen Systemen (z. B. Insulinpumpen oder Smart-Pens zur Insulindosierung) erfüllen, sondern ebenfalls in Bezug auf Genauigkeit und Zuverlässigkeit von Alarmen und Warnungen.
Gleichzeitig wurden neue, strengere Anforderungen zur Messgenauigkeit dieser iCGM-Systeme festgelegt, welche sich an den therapeutischen Implikationen der gemessenen Werte orientieren. So wurde unter anderem festgelegt, dass mehr als 85 % der Vergleichsmessungen mit einem Labormessgerät sich in einem Toleranzbereich von ± 15 mg/dl befinden müssen, wenn die Glukosemessungen Werte unter 70 mg/dl (3,9 mmol/l) ergeben. Im euglykämischen Bereich (70 – 180 mg/dl bzw. 3,9 – 10,0 mmol/l) müssen mindestens 70 %, im hyperglykämischen (> 180 mg/dl bzw. > 10,0 mmol/l) mindestens 80 % der iCGM-Messungen eine Abweichung von maximal 15 % zur Laborreferenz aufweisen. Nicht auftreten dürfen außerdem Blutglukosewerte > 180 mg/dl (10,0 mmol/l), wenn der iCGM-Wert unter 70 mg/dl (3,9 mmol/l) liegt. Des Weiteren darf kein Blutzuckerwert unter 70 mg/dl (3,9 mmol/l) liegen, wenn der dazugehörige iCGM-Wert 180 mg/dl (10,0 mmol/l) überschreitet.
Erstmalig sind zudem Anforderungen an die Genauigkeit der Glukoseänderungsraten festgelegt und das Fehlen von klinisch signifikanten Datenlücken während der gesamten Lebensdauer des Glukosesensors vorgeschrieben. Die Daten zur Genauigkeit sowie zu Änderungsgeschwindigkeiten müssen in der pädiatrischen und der Erwachsenenpopulation übereinstimmen. Weiterhin müssen für alle Daten, welche für den Vergleich zwischen dem iCGM-System und der Referenz verwendet werden, die Proben parallel gesammelt und in einem anerkannten Labor analysiert werden, welches eine international anerkannte Messmethode und Referenzmaterial verwendet. Damit ist die Methodik für die Bestimmung der Genauigkeit eines CGM-Systems festgelegt worden, was eine essenzielle Voraussetzung für die Validität der erhobenen Daten und damit auch deren Vergleichbarkeit darstellt. Aktuell erfüllt nur das Dexcom-G6-rtCGM-System diese hohen Anforderungen [Siegmund 2017].
Es bleibt abzuwarten, wann solche Vorgaben internationale Standards sein und auch in Europa/Deutschland umgesetzt werden.
9. Ausblick
In den letzten Jahren hat eine erhebliche Veränderung bei der Glukosemessmethode durch Menschen mit Diabetes stattgefunden. Nach unserer Einschätzung (es liegen uns keine zuverlässigen Daten vor) nutzen maximal die Hälfte der Patienten mit Typ-1-Diabetes, die eine intensivierte Insulintherapie mit Insulinpens durchführen, regelmäßig ein rtCGM-/iscCGM-System. Unter Patienten, die eine Insulinpumpe nutzen, liegt der Anteil vermutlich noch höher. Bei jüngeren Patienten, insbesondere bei Kindern, sind die Anteile vermutlich deutlich höher. Bei Patienten mit Typ-2-Diabetes ist der Anteil von Nutzern von CGM-Systemen (insbesondere des iscCGM-Systems) zwar relativ betrachtet deutlich niedriger, bedingt durch die große Anzahl von Patienten ist die absolute Zahl der Nutzer allerdings beachtlich (> 1,5 Millionen weltweit).
Insgesamt stellt diese Entwicklung einen fundamentalen Paradigmenwechsel in der Therapie dar (ähnlich dem Wechsel von der Uringlukose- zur Blutglukosemessung), der in den nächsten Jahren vermutlich weitergehen wird. Dabei muss beachtet werden, dass bisher im Gegensatz zur Blutglukosemessung keine weltweit verbindlichen klinischen oder technischen Mindeststandards für rtCGM-/iscCGM-Systeme definiert worden sind. Wir fordern daher, einen technischen wie auch einen klinischen Standard für CGM-Systeme zu etablieren, um klare Rahmenbedingungen für eine sichere Nutzung der Systeme zur Therapieanpassung zu gewährleisten.
10. Praxis-Tipps
Separat von dieser wissenschaftlichen Stellungnahme wurden auf der Homepage der AGDT Praxis-Tipps für Nutzer von Systemen zur kontinuierlichen Glukosemessung veröffentlicht (siehe folgenden Kasten).
AGDT-Vorschlag für "Praktische Hinweise" entsprechend klinischen Erfahrungen zum Ersatz von Blutglukosemessungen durch Messungen mit Systemen zum kontinuierlichen Glukosemonitoring (rtCGM) oder Flash-Glukosemonitoring (FGM) (Glukosemonitoring mit intermittierendem Scannen [iscCGM])
Der Ersatz von Blutzuckermessungen durch rtCGM/iscCGM wird durch Studien unterstützt (Stellungnahme der AGDT zum Ersatz von Blutglukosemessungen durch Messungen mit Systemen zum kontinuierlichen real-time-Glukosemonitoring [rtCGM] oder CGM mit intermittierendem Scannen [iscCGM];), ein vollständiger und unkritischer Ersatz ist jedoch vom Hersteller nicht vorgesehen und ist auch aus klinischer Erfahrung nicht grundsätzlich empfehlenswert. Die CGM-Systeme der Unternehmen Abbott und Dexcom sind zum Ersatz von Blutglukosemessungen in Deutschland/Europa vorgesehen. Das Unternehmen Medtronic hat eine entsprechende Zulassung für sein CGM-System in den USA beantragt.
Praktische Hinweise
1. Schulung
Nutzung der rtCGM-/iscCGM-Systeme nur nach fachkompetenter technischer Einweisung und Teilnahme an einer strukturierten Schulung (Einzel- oder Gruppenschulung).
2. Back-up
Patienten, die CGM-Systeme verwenden, sollten ein Blutzuckermesssystem (Gerät, Teststreifen, Stechhilfe) als Back-up immer mit sich führen, um bei einem Ausfall des CGM-Systems kapilläre Blutglukosewerte bestimmen zu können.
3. Sensorenwechsel
Die Glukosesensoren der CGM-Systeme sollten vorzugsweise zu Zeiten gewechselt werden, in denen die "Run-in"-Phase vom Patienten gut überwacht und verfolgt werden kann.
4. rtCGM
- Kalibrationen nach Herstellerangaben durchführen: das rtCGM-System des Unternehmens Dexcom (Dexcom G4 Platinum und Dexcom G5 Mobile) zweimal täglich kalibrieren.
- Das System Dexcom G6 des Unternehmens Dexcom ist werkskalibriert, eine Kalibration ist möglich, aber nicht zwingend notwendig.
- Nach Anlage des Glukosesensors Dexcom G6 sollten weiterhin Blutzuckermessungen vor jeder Therapieentscheidung erfolgen, bis eine ausreichende Übereinstimmung der Gewebeglukosewerte mit den Blutzuckerwerten beobachtet wird.
- Im praktischen Alltag hat sich eine Kalibration 1 × täglich am Morgen (Dexcom G6) bewährt, um in den meisten Situationen eine gute und stabile Übereinstimmung der Gewebeglukosewerte mit den Blutzuckerwerten zu erreichen.
- Bei Unsicherheiten in Bezug auf die Plausibilität des Messwerts oder bei raschen Glukoseschwankungen Blutzuckerwerte zur Therapieentscheidung heranziehen.
- Bei Patienten, deren Gewebezuckermessungen durch das rtCGM-System wiederholt erheblich von den Blutzuckerwerten abweichen, sind häufigere Blutzuckermessungen erforderlich, insbesondere vor therapeutischen Entscheidungen.
- Die Vorgaben des Herstellers zu zusätzlichen Blutzuckermessungen in bestimmten Situationen sollten umgesetzt werden (siehe Bedienungsanleitungen).
5. iscCGM (FreeStyle Libre/FreeStyle Libre 2)
- Die FreeStyle-Libre- und FreeStyle-Libre-2-CGM-Systeme des Unternehmens Abbott sind werkskalibriert, eine Kalibration ist bei beiden Systemen nicht möglich.
- Blutzuckermessungen sind auch bei Verwendung eines iscCGM-Systems zu folgenden Zeiten empfehlenswert:
- Nach Anlage eines iscCGM-Sensors sollten weiterhin Blutzuckermessungen vor jeder Therapieentscheidung erfolgen, bis eine ausreichende Übereinstimmung der Gewebezuckerwerte mit den Blutzuckerwerten beobachtet wird (besondere Aufmerksamkeit in den ersten 24 Stunden). Während der restlichen Sensorlaufzeit sollten gelegentliche Blutzuckermessungen erfolgen, z. B. einmal täglich.
- Bei Patienten, deren Gewebezuckermessungen wiederholt erheblich von den Blutzuckerwerten abweichen, sind häufigere Blutzuckermessungen erforderlich, insbesondere vor therapeutischen Entscheidungen.
- Die Vorgaben des Herstellers sollten umgesetzt werden: Blutzuckermessungen generell in Phasen mit rasch schwankendem Glukosespiegel, zur Bestätigung einer vom CGM-System angezeigten Hypoglykämie oder drohenden Hypoglykämie und wenn die Symptome nicht mit den von dem iscCGM-System angezeigten Glukosewerten übereinstimmen.
Auszüge aus den Bedienungsanleitungen
Bedienungsanleitung Dexcom G5 Mobile
Blutglukosemessungen sollen weiterhin durchgeführt werden:
Therapieentscheidungen dürfen mit diesem System nur getroffen werden:- wenn die Glukosewarnungen und Glukosemesswerte mit den Symptomen oder Erwartungen übereinstimmen.
- wenn die Geräteanweisung befolgt wird und das Gerät alle 12 Stunden nach der Anfangskalibration kalibriert wurde.
- auf Grundlage des Gewebeglukosewerts, des Trendpfeils, des Trenddiagramms und/oder der umsetzbaren Warnungen.
- wenn mindestens drei aufeinanderfolgende Werte aus den letzten 15 Minuten vorhanden sind.
Bedienungsanleitung Dexcom G6
Blutglukosemessungen sollen weiterhin durchgeführt werden:- Egal ob Sie ein neuer oder bereits erfahrener Anwender von Dexcom sind, sollten Sie Ihr Blutzuckermessgerät weiterhin nutzen, um Behandlungsentscheidungen zu treffen, bis Sie wissen, wie Dexcom für Sie funktioniert.
- Kein Wert, kein Pfeil, keine CGM-basierte Behandlungsentscheidung.
- Ihre Symptome stimmen nicht mit den Messungen des G6 überein.
- Nutzen Sie Ihr Blutzuckermessgerät, wenn Sie unsicher sind.
Benutzerhandbuch des iscCGM-Systems FreeStyle Libre Rev. (04/2014)
Blutglukosemessungen sollen weiterhin durchgeführt werden:- in Phasen mit rasch schwankendem Glukosespiegel.
- zur Bestätigung einer vom Sensor berichteten Hypoglykämie oder drohenden Hypoglykämie.
- wenn die Symptome nicht mit dem Messwert des FreeStyle Libre Flash Glukose Messsystems übereinstimmen.
Benutzerhandbuch des iscCGM-Systems FreeStyle Libre 2
SMBG sollen weiterhin durchgeführt werden:- in Phasen mit sich schnell ändernden Glukosewerten (mehr als 2 mg/dl pro Minute).
- Um vom Sensor gemeldete Hypoglykämie oder drohende Hypoglykämie zu bestätigen.
- Ignorieren Sie keine Symptome, die möglicherweise Folgen eines niedrigen oder hohen Blutzuckers sind.
- Wenn Ihre Symptome nicht mit dem gemessenen Sensor-Glukosewert übereinstimmen.
- Wenn Sie den Verdacht haben, dass Ihr Messwert ungenau ist.
Wichtig für den Nutzer:
Besonders am Tag des Legens eines neuen Glukosesensors sind die Messwerte von rtCGM- und iscCGM-Systemen mit Zurückhaltung für Therapieentscheidungen zu verwenden. Bei den neueren CGM-Systemen – wie Dexcom G6 und FreeStyle Libre 2 – ist die Messgüte am ersten Tag besser als bei den früheren Systemen. Sollten während der Nutzung des rtCGM-/iscCGM-Systems Zweifel an der Messgüte des aktuellen Glukosesensors auftreten, sind Blutzuckerselbstmessungen zur Abklärung dringend anzuraten. Bei dem iscCGM-System ist ein Blutzuckermessgerät in dem Lesegerät integriert.
Ein weiteres Problem stellt bei plötzlichem dauerhaftem Ausfall des Glukosesensors oder des Lesegeräts die Wiederbeschaffung des Medizinprodukts dar:- Neue Sensoren/Lesegeräte für das iscCGM-System werden in erster Linie über ein Online-Portal bestellt. Die Sensoren des iscCGM können auch alternativ über eine App mit einem Smartphone gescannt werden.
- rtCGM-Sensoren werden beim Hersteller über eine Hotline oder online bestellt oder der Patient hat eine Verordnung, mit der er sich die Sensoren bei einem Lieferanten besorgen kann. Auch hier ist es möglich, bei Ausfall des Lesegeräts alternativ eine App im Smartphone als Empfangsgerät zu nutzen.
- Blutglukoseteststreifen sind auch am Wochenende und kurzfristig in jeder Apotheke erhältlich.
Was unterscheidet die 2. Generation des iscCGM-Systems von einem rtCGM-System?
In dem G-BA-Beschluss aus dem Jahr 2016 zur Kostenerstattung von rtCGM-Systemen wird eine detaillierte Anforderungsliste an die technische Leistungsfähigkeit solcher Systeme gegeben:- kontinuierliche Glukosemessung mittels eines Sensors in der interstitiellen Flüssigkeit des Unterhautfettgewebes,
- automatische Übermittlung des Messergebnisses mittels Transmitters an ein Empfangsgerät,
- kontinuierliche Anzeige der Messwerte und der Trends zum Glukosegehalt,
- mit einer Alarmfunktion mit individuell einstellbaren Grenzen warnt das Gerät vor dem Erreichen zu hoher oder zu niedriger Glukosewerte.
Die grundsätzlichen Unterschiede des iscCGM-Systems der 1. Generation zu den rtCGM-Systemen waren:
- keine automatische Übermittlung der Glukosewerte an ein Empfangsgerät,
- erforderlicher Scan mit dem Empfangsgerät zur Darstellung der Glukosewerte,
- keine kontinuierliche Anzeige der Messwerte und Trends,
- keine Alarmfunktion.
- keine automatische Übermittlung der Glukosewerte an ein Empfangsgerät,
- erforderlicher Scan mit dem Empfangsgerät zur Darstellung der Glukosewerte auch bei Alarmen,
- keine kontinuierliche Anzeige der Messwerte und Trends,
- Alarmfunktion ohne kontinuierliche Anzeige der Messergebnisse.
Die Frage ist: Stellt die 2. Generation eine "rtCGM-Variante light" dar? Zur Beurteilung dieser Frage hilft die Auflistung der Eigenschaften von rtCGM-Systemen und der Eigenschaften der beiden Generationen des iscCGM-Systems (siehe oben). Demnach erfüllt im strengen Sinn die 2. Generation des iscCGM nicht die Anforderungen des G-BA-Beschlusses für ein rtCGM-System. Eine aktuelle Entscheidung des GKV-Spitzenverbands hat einen Antrag auf Listung von FreeStyle Libre 2 im Hilfsmittelverzeichnis positiv beschieden. Ein G-BA-Beschluss steht hierzu noch aus.
Aber auch im G-BA-Beschluss von 2016 nicht berücksichtigte Faktoren, die rtCGM-Systeme beherrschen, weist das iscCGM der 2. Generation nicht auf. Alle aktuell verfügbaren rtCGM-Systeme müssen oder können bei Bedarf kalibriert werden. Diese Möglichkeit der Kalibration gibt dem Nutzer die Chance, voneinander abweichende Gewebeglukose- und Blutglukosewerte anzugleichen. Dies ist ein wichtiger Aspekt bei der Nutzung von Automated-Insulin-Delivery (AID)-Systemen zur automatischen Steuerung der Insulinzufuhr mittels einer Insulinpumpe. Aber auch abweichende Messergebnisse zwischen Blut- und Gewebezucker können so bei individuellen Fehlern korrigiert werden, z. B. bei fehlender Messgüte einiger Glukosesensoren. Diese Möglichkeit zur Kalibration bietet das iscCGM-System nicht; es ist ausschließlich werkskalibriert. Der Vorteil einer Werkskalibration ist, dass Fehler durch falsche Kalibration vermieden werden.
Des Weiteren ist bei einer Hypoglykämie ein weiterer Schritt zur Generierung des Glukosewerts erforderlich. Nachdem das iscCGM-System Alarm meldet, muss ein Scan durchgeführt werden, um den aktuellen Glukosewert anzuzeigen. In einer Hypoglykämie sind "komplexe" Handlungen schwer umzusetzen und sollten daher möglichst vermieden werden.
Die Frage, welche Patienten ein rtCGM-System brauchen und für welche ein iscCGM-System ausreichend ist, wird der behandelnde Diabetologe zu klären haben und ist individuell zu entscheiden.
Erschienen in: Diabetes, Stoffwechsel und Herz, 2019; 28 (4) Seite 206-217

