Parodontale Entzündung und Diabetes mellitus sind bidirektional miteinander verknüpft [Skamaga 2008, Preshaw 2012, Chapple 2013, Pfützner 2023]. Während Hyperglykämie das parodontale Risiko erhöht [Tsai 2002, Mealy 2006], trägt eine aktive orale Entzündung zur systemischen Low-grade-Inflammation und Insulinresistenz bei [Hotamisligil 2006, Engebretson 2013, Schenkein 2013]. Daher spielt die Mundgesundheit eine große Rolle bei der ganzheitlichen Betreuung von Menschen mit Diabetes und die Erkennung von parodontalen Schäden ist ein wichtiger Baustein für eine gute und nachhaltige Prognose [IDF 2009]. Klassische Parodontal-Scores erfassen hauptsächlich eingetretene anatomische Strukturschäden [Tonetti 2018]. aMMP-8 (aktivierte Matrix-Metalloproteinase-8) weist dagegen aktuelle kollagenolytische Aktivität nach und ist damit für Prävention und Therapie-Monitoring in der Diabetologie besonders relevant [Al-Majid 2018, Lätheenmaki 2018, Sorsa 2020, Deng 2021, Sorsa 2022, Wei 2024].
Zusammenfassung
Eine aktive parodontale Entzündung trägt zur systemischen Inflammation bei, verschärft die Insulinresistenz und erhöht das kardiovaskuläre Risiko bei Menschen mit Diabetes. Ziel dieses Papiers ist es, ein praxistaugliches Vorgehen für die Anwendung der aMMP-8-Speicheldiagnostik in der Diabetologie darzustellen – von Screening und Befundinterpretation bis zur konkreten Handlungsableitung. Die Empfehlungen basieren auf einer Nominal-Group-Technique-gestützten Konsensusfindung und einer Evidenzzusammenführung aus Zahnmedizin, Innerer Medizin und Diabetologie.aMMP-8 ist ein Prozessmarker der akuten Gewebezerstörung im Parodont; regelmäßige, nicht-invasive Point-of-Care-Messungen im Speichel lassen sich ohne Mehraufwand in DMP-Abläufe integrieren. Bei auffälligem Befund folgt eine standardisierte Rückmeldung an die Zahnmedizin mit klaren Überweisungspfaden und Re-Test-Terminierung; die Befundverläufe werden gemeinsam mit hsCRP/HbA1c zur Therapieführung herangezogen. So unterstützt die aMMP-8-Speicheldiagnostik die Erreichung metabolischer und kardiovaskulärer Zielwerte, ermöglicht ein frühzeitiges, ursachenorientiertes Eingreifen und kann helfen, pharmakologische Eskalationen zu vermeiden.
Einleitung
aMMP-8 wird überwiegend von neutrophilen Granulozyten freigesetzt und spaltet als aktivierte Kollagenase Typ-I-Kollagen in der parodontalen Extrazellulärmatrix, wodurch kollagenolytische Prozesse im Zahnhalteapparat vorangetrieben werden [Romanelli 1999, Kuula 2009, Al-Majid 2018, Sorsa 2022]. Die hierdurch begünstigte Störung der oralen Barriere erleichtert das Eindringen mikrobieller Produkte und von Matrixabbaufragmenten in das Gewebe und in die Zirkulation. Dies aktiviert Mustererkennungswege und fördert proinflammatorische Zytokinantworten, insbesondere Interleukin (IL)-6 und Tumornekrosefaktor (TNF)-α, die die Insulin-Signaltransduktion hemmen und so die Insulinresistenz erhöhen [Hotamisligil 2006, Schenkein 2013, Vitkov 2023, Aji 2024, Neurath 2024]. Bei Menschen mit Diabetes akkumuliert diese chronische Entzündungslast ("Low-grade-Inflammation") und trägt zur Progression kardiometabolischer Komorbiditäten bei, einschließlich Atherosklerose-Fortschritt und erhöhter kardiovaskulärer Ereignisraten [Pussinen 2004, Loos 2005, Saremi 2005, Pussinen 2007, Tonetti 2013, Lai 2025].
Bei Menschen mit Diabetes treten parodontale Erkrankungen häufiger und schwerer auf, gehen mit einer schlechteren glykämischen Kontrolle einher und sind mit höheren Komplikationsraten assoziiert [Saremi 2005, Skamagas 2008, Teeuw 2010, Preshaw 2012, Chapple 2013]. Für die Detektion aktueller parodontaler Aktivität steht der aMMP-8-Point-of-Care-Test zur Verfügung, der zwischen periodontaler Gesundheit und aktiver Entzündung zuverlässig unterscheidet und sich für Screening und Verlaufsbeurteilung eignet [Sorsa 2020, Deng 2021, Lähteenmäki 2021, Sorsa 2022, Wei 2024]. Interventionsstudien zeigen zudem, dass eine konsequente Parodontaltherapie kurzfristig systemische Entzündungsmarker senken und die Insulinresistenz verbessern kann [Engebretson 2013]. Leitlinien und Empfehlungen betonen daher regelmäßige Mundhöhlen-Checks in der Diabetesversorgung; aMMP-8 ergänzt diese Strategie als objektiver Prozessmarker der kollagenolytischen Aktivität und unterstützt Prävention sowie Therapie-Monitoring [IDF 2009, Sorsa 2020, Sorsa 2022].
Ziel einer interdisziplinären Konsensus-Arbeitsgruppe des Gesundheitssenats der deutschen Mundgesundheitsstiftung war es in den Jahren 2024/2025, Vorschläge für den praktischen Einsatz von aMMP-8-Messungen bei der Langzeitbetreuung von Patienten mit chronisch-systemischen Grunderkrankungen in den wichtigsten Indikationsgebieten zu erarbeiten und ergebnisorientierte Empfehlungen für weitergehende diagnostische oder therapeutische Maßnahmen zu geben. Die Konsensusfindung wurde mit Hilfe der Nominal-Group-Technique durchgeführt [Mullen 2021]. Hier berichten wir über die Ergebnisse der Konsensusfindung für Patienten mit Diabetes mellitus.
Indikationen und Messzeitpunkte
Die aMMP-8-Speichelmessung sollte regelhaft in die Diabetesbetreuung integriert werden: Als Routinemessung empfiehlt sich ein Intervall von etwa sechs Monaten im Rahmen der DMP-Kontrollen (Disease-Management-Programm), bei stabilen Verläufen mindestens einmal pro Jahr. Anlassbezogen ist eine Bestimmung sinnvoll, wenn HbA1c-Ziele trotz guter Adhärenz verfehlt werden, der antidiabetische Therapiebedarf unerwartet steigt, systemische Entzündungsmarker wie hochsensitives C-reaktives Protein (hsCRP) oder IL-6 persistierend erhöht sind, vor Beginn bzw. unter laufender Immunmodulation sowie bei kardiovaskulären Hochrisikokonstellationen.
Praxis-Algorithmus
Im diabetologischen Alltag erfolgt zunächst eine aMMP-8-Bestimmung im Speichel am Point-of-Care. Anschließend wird das Ergebnis interpretiert: Liegt der Wert im Normbereich, erfolgt die Weiterbetreuung im Routine-Recall nach sechs bis zwölf Monaten im Rahmen der DMP-Kontrollen; Präventions- und Prophylaxemaßnahmen werden fortgeführt. Bei erhöhtem aMMP-8-Wert sollten zeitnah eine Dentalhygiene bzw. Parodontaltherapie mit Sanierung und Mundhygiene-Coaching eingeleitet werden, gefolgt von einem Re-Test nach sechs bis zwölf Wochen. Normalisieren sich die Werte, kehrt der Patient in das Routine-Intervall zurück; bleiben sie erhöht, wird interdisziplinär nach weiteren Entzündungsquellen gesucht (z. B. Hals-Nasen-Ohren, Dermatologie, Urogenital-/Gastrointestinal-Trakt, Implantate, chronische Wunden) und internistisch weiter abgeklärt (siehe Abbildung 1). Unabhängig vom Pfad empfiehlt sich ein strukturiertes Outcome-Tracking (aMMP-8, hsCRP/IL-6, HbA1c bzw. Time-in-Range, Insulindosis/Medikation, Infekt-/kardiovaskuläre Ereignisse).
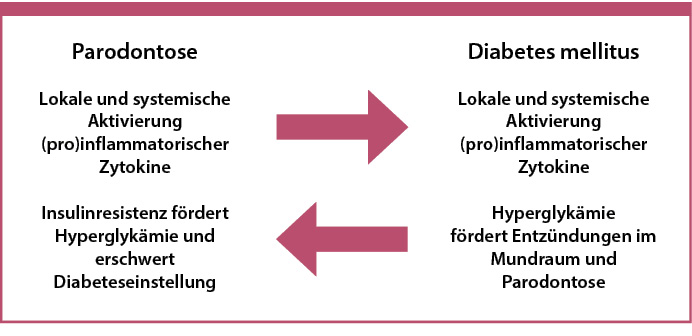 Abb. 1: Bidirektionale Beeinflussung von Diabetes und Parodontose.
Abb. 1: Bidirektionale Beeinflussung von Diabetes und Parodontose.
Bei Ankunft in der Praxis erfolgt der aMMP-8-Test als standardisierter Eingangsschritt (Check-in), idealerweise noch vor der Vitalzeichen-Erhebung, sodass das Ergebnis zum ärztlichen Gespräch vorliegt. Die Entnahme (Mundspül-/Sulkusprobe) wird durch Medizinische Fachangestellte nach Standardarbeitsanweisung (Standard Operating Procedure, SOP) durchgeführt; Ergebnisvalidierung und Plausibilitätscheck (Kontrollfeld, Verfallsdatum, Dokumentationsvollständigkeit) sind Teil der Routine. Das Resultat wird unmittelbar in die Patientenakte übertragen und auf einem Ampel-Befundblatt zusammengefasst:
- "Grün" (unauffällig) mit Routine-Recall
- "Gelb" (grenzwertig/erhöht) mit strukturierter Mundhygieneberatung und Re-Test-Empfehlung
- "Rot" (deutlich erhöht) mit Priorisierung einer zahnmedizinischen Abklärung
Im ärztlichen Gespräch wird der Befund in den Gesamtbefund integriert (Glykämie, hsCRP/IL-6, kardiovaskuläres Risiko), Therapieziele werden gemeinsam festgelegt und die Patienten erhalten eine kurze, verständliche Befunderläuterung zum Mitnehmen.
Die Kommunikation mit der Zahnmedizin erfolgt über ein standardisiertes Rückmeldeformular, das Parodontalstatus (Parodontaler-Screening-Index (PSI)/Stage/Grade), aktive Therapie, adjuvante Empfehlungen und einen vorgeschlagenen Re-Test-Zeitraum (typisch 6 – 12 Wochen nach Intervention) umfasst. Feste Überweisungspfade sichern kurze Wege: Die Praxis terminiert bereits beim Check-out den zahnärztlichen Ersttermin sowie den internen Re-Test; beide Termine werden im Recall-System hinterlegt und automatisiert erinnert. Rückläufe aus der Zahnmedizin werden der Akte zugeordnet und im nächsten Arztgespräch besprochen; bei Persistenz erhöhter Werte wird eine strukturierte Suche nach weiteren Entzündungsquellen initiiert (siehe Abbildung 2).
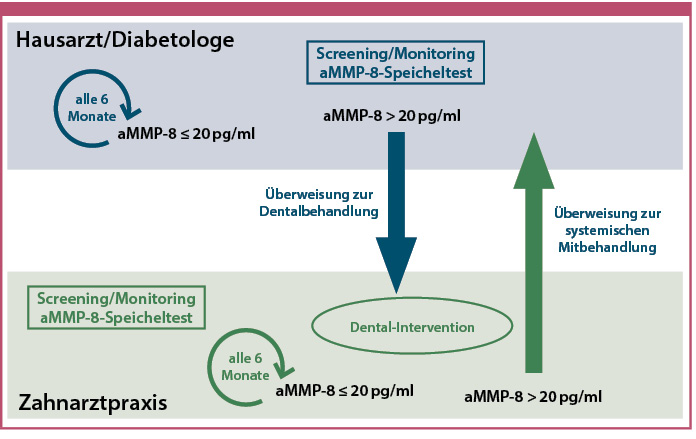 Abb. 2: Vereinfachtes Schema zur interdisziplinären Kooperation zwischen Diabetologie und Zahnheilkunde.
Abb. 2: Vereinfachtes Schema zur interdisziplinären Kooperation zwischen Diabetologie und Zahnheilkunde.
Fallbeispiel
Ein 58-jähriger Patient mit Typ-2-Diabetes (Body-Mass-Index [BMI] 31 kg/m²) und Begleiterkrankungen (metabolische Dysfunktions-assoziierte steatotische Lebererkrankung [MASLD], koronare Herzkrankheit [KHK]) stellt sich mit suboptimaler Stoffwechselkontrolle unter Metformin-Monotherapie (500 mg, 1 – 0 – 1) vor (HbA1c 6,9 %). Entzündungsparameter sind erhöht (hsCRP 4,2 mg/l), der aMMP-8-Schnelltest fällt pathologisch aus (58 ng/ml). Klinisch bestehen keine akuten dentalen Beschwerden. Im Rahmen des intersektoralen Vorgehens erfolgen zeitnah eine professionelle Dentalhygiene mit initialer parodontaler Therapie sowie eine strukturierte Mundhygiene-Schulung; die Diabetestherapie bleibt unverändert.
Nach acht Wochen zeigen sich aMMP-8 (< 20 ng/ml) und hsCRP (< 1 mg/l) normalisiert; zugleich verbessert sich der HbA1c-Wert ohne Pharmaka-Eskalation auf 6,2 %. Der Befund wird im Verlauf bestätigt (Recall/Re-Test), die Metformin-Dosis bleibt stabil.
Die Fallentwicklung stützt die Annahme, dass die Kontrolle oraler Entzündung zur systemischen Entzündungsreduktion beiträgt und die glykämische Stoffwechselkontrolle unterstützen kann, ohne Kausalität im Einzelfall abschließend zu beweisen.
Qualitätssicherung
Zur Qualitätssicherung der aMMP-8-Speicheldiagnostik sind präanalytische Standards entscheidend: Proben werden möglichst zur gleichen Tageszeit entnommen, ideal vor Mundpflege, Essen/Trinken und ohne vorherige Mundspüllösungen. Akute Infekte der oberen Atemwege, fieberhafte Erkrankungen, jüngste zahnärztliche Eingriffe, starke Blutungen, Nikotinkonsum kurz vor der Probe sowie intensive körperliche Belastung werden dokumentiert, da sie Werte beeinflussen können. Die Probenahme erfolgt nach einheitlichem Schema (Instruktion, Sammeldauer/-technik), mit Chargen- und Ablaufkontrolle der Testmaterialien und dokumentierter Geräte-/App-Version.
Bei der Interpretation ist zu berücksichtigen, dass aMMP-8 ein Prozessmarker akuter Kollagenolyse ist und nicht krankheitsspezifisch: Er zeigt aktive Gewebezerstörung an, ohne eine Parodontitis zu "stagen" oder zu "graden". Erhöhte Werte können auch bei anderen oralen Entzündungsquellen auftreten (z. B. Gingivitis, periimplantäre Mukositis) und müssen klinisch/dental korreliert werden. Umgekehrt schließen Normwerte eine parodontale Vorschädigung nicht aus, insbesondere in inaktiven Phasen. Der Befund ersetzt daher nicht Anamnese, klinische Inspektion und parodontale Basisdiagnostik, sondern ergänzt sie.
Für die Verlaufsbeurteilung gilt: Wiederholungsmessungen erfolgen unter möglichst identischen Bedingungen (gleiche Tageszeit, Nüchtern-/Hygienestatus, identisches Lesegerät/Reader) und mit konsistenter IT-Dokumentation (Zeitpunkt, Kontext, Komedikation, Infekte, Zahnarzttermine). Geräte werden regelmäßig kalibriert, interne Qualitätskontrollen protokolliert und Lot-Wechsel nachvollziehbar abgelegt; ideal ist die Teilnahme an externer Qualitätssicherung/Ringversuchen. Cut-off-basierte Ampelberichte werden stets zusammen mit klinischen Parametern (z. B. Blutungsneigung, Plaque-Index) sowie systemischen Markern (hsCRP) und Stoffwechselzielen (HbA1c, Insulinbedarf) bewertet. Grenzwertige oder unerwartete Befunde sollten nach sechs bis zwölf Wochen unter standardisierten Bedingungen verifiziert werden; persistierende Erhöhungen ohne oralen Fokus triggern die Suche nach weiteren Entzündungsquellen. Datenschutz und Zugriffsrechte für die interprofessionelle Befundweitergabe sind geregelt (DMP-/Praxis-IT). Limitationen sind hierbei: eine biologisch interindividuelle Streuung, mögliche Störfaktoren (z. B. Rauchstatus, Schwangerschaft, Immunsuppression), fehlende Aussage zur Langzeitprogression – daher immer die Kombination aus aMMP-8, klinischem Befund und systemischem Kontext nutzen.
Integration der aMMP-8-Messung ins DMP
Eine strukturierte Jahresplanung erleichtert die Integration in bestehende DMP-Abläufe: aMMP-8 wird routinemäßig im Rahmen der halbjährlichen DMP-Kontrollen erhoben (bei stabilen Verläufen mindestens 1×/Jahr). Anlassbezogene Zusatzmessungen erfolgen bei HbA1c-Zielverfehlung trotz Adhärenz, steigendem Therapiebedarf, persistierend erhöhtem hsCRP/IL-6, vor bzw. unter Immunmodulation sowie in kardiovaskulären Hochrisikokonstellationen. Bei erhöhtem Befund werden feste Überweisungspfade zur Zahnmedizin aktiviert; nach Dentalhygiene/Parodontaltherapie erfolgt ein Re-Test nach sechs bis zwölf Wochen unter identischen Testbedingungen. Persistiert die Erhöhung ohne oralen Fokus, wird systematisch nach weiteren Entzündungsquellen gesucht. Eine IT-gestützte Recall-Logik dokumentiert Messzeitpunkte, Befundtrends (Ampelblatt) und Rückmeldungen aus der Zahnmedizin und erinnert automatisiert an Re-Tests.
|
|
Erschienen in: Diabetes, Stoffwechsel und Herz, 2026; 35 (2) Seite 101-104


