Die Mikroangiopathie wird oft als Schicksalserkrankung bei Menschen mit Diabetes bezeichnet. Mikroangiopathische Schäden verursachen beispielsweise Nephropathie oder Retinopathie. Doch man kann etwas dagegen unternehmen, wie Dr. Gerhard-W. Schmeisl weiß.
Die Mikroangiopathie als Schicksalserkrankung bei Menschen mit Diabetes hat in den letzten Jahren wieder an Bedeutung gewonnen. Die beiden wichtigsten Erkrankungen bzw. Komplikation bei Menschen mit Diabetes durch mikroangiopathische Schäden sind nach wie vor die diabetische Nephropathie und die diabetische Retinopathie.
So haben neue diagnostische und therapeutische Möglichkeiten die Häufigkeit der makrovaskulären Komplikationen reduzieren geholfen – der Herzinfarkt, die Herzinsuffizienz und der Schlaganfall, neuerdings auch der Krebs – stehen aber häufig noch im Vordergrund des therapeutischen Interesses bei Menschen mit Diabetes.
Dabei ist z.B. die Niereninsuffizienz immer noch die häufigste Ursache für ein chronisches Nierenversagen in den westlichen Industrienationen. Die diabetische Retinopathie wird häufig erst dann diagnostiziert, wenn Symptome auftreten – diese sind dann meist schon Zeichen eines fortgeschrittenen Stadiums einer Retinopathie – warum also nicht schon ein viel früheres, rechtzeitiges Screening, zumal immer bessere Möglichkeiten der Therapie gerade in frühen Stadien bestehen.
Die diabetische Retinopathie ist laut deutschem Gesundheitsbericht Diabetes 2022 (Hannes, Lemmen 22) neben den 3 häufigsten Augenerkrankungen weltweit wie Glaukom, Katarakt und altersabhängiger Makuladegeneration, immer noch eine ernst zu nehmende Erkrankung mit der Gefahr der frühen Erblindung trotz unserer heutigen Möglichkeiten.
Mikroangiopathie - was ist das?
Von einer Mikroangiopathie spricht man, wenn die kleinsten Blutgefäße betroffen sind, die unmittelbar ein Organ in der Endstrombahn mit Blut versorgen, bei Menschen mit Diabetes – von einer diabetischen Mikroangiopathie. Diese betrifft insbesondere die Kapillaren – dies kann zu diabetes-spezifischen Erkrankungen führen, der
- Diabetischen Nephropathie
- Diabetischen Retinopathie
Beteiligt ist sie auch an der Entstehung:
- Der Diabetischen Polyneuropathie
- Der Diabetischen Kardiomyopathie
- Des diabetischen Fußsyndroms (zusammen mit der peripheren arteriellen Verschlusskrankheit und der Polyneuropathie)
Pathogenese der Mikroangiopathie
Das Wesen der Mikroangiopathie besteht in einer Verdickung der kapillären Basalmembran einer Arterie, durch eine meist längere Hyperglykämie und einer dadurch bedingten nicht-enzymatischen Glykosilierung von Eiweißen der Basalmembran. Die Dicke der Basalmembran korreliert mit der Dauer sowie der Einstellungsgüte des Diabetes und – wie wir heute wissen – einer genetischen Disposition (z.B. mehr Männer als Frauen betroffen!).
Während die Atheromatose der großen Blutgefäße nicht eine direkte Folge des Diabetes und der Blutzuckereinstellung ist, hängt die Mikroangiopathie direkt mit der Güte der Blutzuckereinstellung zusammen.
Weitere Ursachen werden angenommen bzw. sind gesichert:
- Bildung von "Zucker-Eiweiß-Verbindungen" (AGE’s (= Advanced glycation end products), die eine Schädigung der Gefäßwand bewirken.
- So genannter "Oxidativer Stress" z.B. durch Rauchen etc. gefördert
- Bestimmte Alkohol-Stoffwechselwege werden gefördert (=Polyolstoffwechsel)
- Aktivierung eines bestimmten Eiweißes der Proteinkinase C (Enzym)
- Durch ihre Hemmung versucht man eine Verbesserung der Durchblutung in den feinsten Ästen der Kapillaren von Netzhaut, Nieren und Nerven zu erreichen!
- Ein früher Verlust der pulsatilen Insulinsekretion (8 bis 12 x/ Stunde sind normal) könnte zu Mikrozirkulationsstörungen sowohl beim Typ 1 als auch beim Typ 2 Diabetes beitragen = Verlust der Sensibilität der vaskulären Insulinrezeptoren mit mangelnder Fähigkeit zur Vasodilatation (NO- vermittelt!) (Pørksen N,2002/Bergsten 2000, Forst 2009).
Die diabetische Nephropathie
2017 hat man weltweit etwa 697 Millionen Menschen mit einer chronischen Nierenerkrankung registriert, das entspricht einer Erkrankungshäufigkeit von 9,7%. Im Vergleich zum Jahr 1990 entspricht dies einem Anstieg um 29,3% - gleichzeitig nahm die Sterblichkeit um 41,5% zu (Galle et al 2021). Unter einer chronischen Nierenerkrankung versteht man eine dauernde Schädigung der Nieren mit einer Abnahme der Glomerulären Filtrationsrate (GFR) und/oder einer erhöhten Ausscheidung des Eiweißes Albumin im Urin (Fraser 2016).
Eine Abnahme der Nierenfunktion gibt es natürlich auch mit zunehmendem Alter – diese wird beschleunigt durch zusätzliche Erkrankungen wie einen Diabetes, Bluthochdruck und Übergewicht /Adipositas und natürlich auch einer Erkrankung der Nieren selbst. Verbunden damit ist ein deutlich erhöhtes Risiko für schwerwiegende Herz – Kreislauf – Erkrankungen mit einer erhöhten Sterblichkeit (Gunnevoort 2013). Die Diagnose einer chronischen Nierenerkrankung beruht auf festen Kriterien und Klassifikationen, die die zuständigen Fachgesellschaften im Laufe der Jahre immer wieder neu festgelegt haben. Neben der arteriellen Hypertonie gilt der Diabetes mellitus als einer der häufigsten Ursachen für eine chronische Nierenerkrankung
Die aktuellen Definitionen stammen aus 2012 = Leitlinie der KDIGO (The Kidney Disease: Improving Global Outcomes). Diese sind notwendig, um eine "moderne" aussagefähige Anleitung für eine Diagnose und damit auch für die Behandlung der chronischen Nierenerkrankungen zu geben.
Was ist eine chronische Nierenerkrankung?
1. Es muss eine krankhafte Nierenfunktion bzw. abnorme Nierenstruktur vorliegen
2. Sie muss länger als 3 Monate andauern
3. Es muss einer der folgenden Parameter vorhanden bzw. eingeschränkt sein:
a. Die GFR =Glomeruläre Filtrationsrate <60ml/Min/1,73m² (Serum-Kreatinin) = Filterfunktion der Niere
b. Albuminurie (Eiweißausscheidung im Urin: ≥30mg/24h oder das Albumin-Kreatinin-Verhältnis (= Albumin to creatine ratio) ACR ≥30mg/g
c. Andere Hinweise auf eine Schädigung
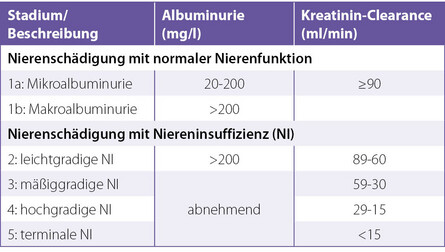
Als beste Kriterien für die Diagnose gilt aktuell: Das Serum Kreatinin und die UACR im Urin werden im Abstand von 3 Monaten gemessen und die Stadien anhand einer Tabelle bestimmt. Als sicherer Hinweis für ein Fortschreiten der Erkrankung gilt eine Abnahme der GFR von über 25% vom Ausgangswert. Die UACR (= Urin Albumin Kreatinin Ratio) wird gegenwärtig immer mehr zur Diagnose einer diabetischen Nephropathie eingesetzt. Während es schon lange möglich ist die e- GFR (= estimated Glomerula Filtration ratio = die geschätzte GFR) sicher im Labor zu bestimmen, ist die Albuminbestimmung im Urin mit einem Teststreifen bisher immer mit einem Fehler behaftet – es wird nicht die Urin – Konzentration (= spezifisches Gewicht) berücksichtigt. Es gibt aktuell jedoch schon Messsysteme, die dies berücksichtigen – so wird eine recht genaue Einschätzung der verbliebenen Nierenfunktion besser und sicherer möglich! Eine weitere Methode die Filterleistung zu untersuchen, ist die Bestimmung des Cystatin C. Dies ist ein körpereigenes Eiweiß, das in bestimmten Situationen zur Bestimmung der glomerulären Filtrationsrate verwendet wird- besonders wenn noch kein Albumin vorliegt. Es wird weniger von äußeren Einflüssen beeinflusst, wie z.B. von der Muskel-Ausstattung eines Menschen (z.B. auch wird so ein erhöhtes Kreatinin bei Body-Buildern bei normalem Cystatin C relativiert!).
Die e-GFR und UACR müssen zur genaueren Bestimmung des Schadens getrennt bewertet werden (L. Merker 2021).

Die diabetische Nephropathie - Besonderheiten
Diabetische Nierenschäden sind die häufigste Ursache in den Industrienationen für eine chronische Nierenschwäche. Sie ist mit eine der häufigsten und auch der gefährlichsten Komplikationen des Diabetes. Etwa 20-40% aller Menschen mit Diabetes entwickeln sie im Laufe ihrer Erkrankung. Das Risiko für eine diabetische Nephropathie ist, wie aus Studien hervorgeht, sowohl beim Typ 1 als auch beim Typ -2 -Diabetes etwa gleich. Bisher spricht man von einer beginnenden diabetischen Nephropathie wenn kleinste Spuren von Eiweiß, mehr als 30mg/dl (Mikroalbuminurie), im Urin auftreten oder eine Einschränkung der Nierenfunktion (<60ml/Min/1,73m² Oberfläche) auftritt. Die Beachtung der Mikroalbuminurie ist deshalb so wichtig, da sie mit einer deutlichen Steigerung der Sterblichkeit für Herz-Kreislauferkrankungen verbunden ist – Gleiches gilt auch für die Einschränkung der Funktion der Nieren, berechnet durch die Filtration (GFR).
Typ -1- Diabetiker sollten ab dem 5.Jahr nach Diagnosestellung mindestens 1x jährlich, Typ -2 -Diabetiker unmittelbar nach der Diagnosestellung und dann auch mindestens 1x jährlich bezüglich eines chronischen Nierenschadens gescreent werden (Leitlinie der DDG, Oktober 2021).
Eine anfangs sogar gesteigerte Filtrationsleistung der Niere (= Hyperfiltration) führt schließlich über eine vermehrte Eiweißausscheidung zu einer Abnahme dieser Funktion!
Die klassischen Veränderungen an der Niere beim Typ 1 Diabetiker nennt man nach ihrem Erstbeschreiber "Kimmelstiel-Wilson-Nephropathie". Es sind typische Veränderungen an der Niere selbst. Bei Menschen mit Typ -2- Diabetes sind dagegen häufig noch andere Erkrankungen, ursächlich vorhanden nämlich eine Hypertonie, sowie Fettstoffwechselstörungen und eine erhöhte Harnsäure.
Während beim Typ 1 Diabetiker für das Aufhalten des Fortschreitens des diabetischen Nierenschadens die Blutzuckerkontrolle die entscheidende Rolle spielt, muss bei Typ 2 Diabetes konsequent der Blutdruck, die Fettstoffwechselstörung und das Gewicht sowie die Harnsäureerhöhung im Blut berücksichtigt werden, um ein Fortschreiten Richtung Niereninsuffizienz zu verhindern. Denn mit zunehmender Niereninsuffizienz steigt auch die kardio-vaskuläre Mortalität (Gansevoort 2012, Go 2004, Tonelli 2012). Nur wenige Patienten mit schweren Herz-Kreislauf-Komplikationen erreichen deshalb auch das Stadium der terminalen Niereninsuffizienz (etwa 2-3%) (Brancati 1997/Morten 2020). Eine weltweite epidemiologische Studie (Cheng ,2021) zeigte, dass die Anzahl dialysepflichtiger Menschen mit Diabetes in den Jahren von 2000-2015 um das 2,7-fache angestiegen ist.
In Studien zeigte sich für Typ-1-Diabetiker ein Zusammenhang zwischen der Diabetesdauer und der zunehmenden Funktionseinschränkung der Nieren. Bei Typ 2 Diabetikern bestand eher ein Zusammenhang mit dem Lebensalter – wahrscheinlich eine zunehmende Nierenfunktionseinschränkung durch die Nephrosklerose im Rahmen des metabolischen Syndroms (H.Schmechel, R.Fünfstück 3/22 Diabetes Stoffwechsel &Herz).
Therapie Ansätze
Basis-Maßnahmen
Basismaßnahmen bei Menschen mit Diabetes und beginnender Niereninsuffizienz sind:
- die Einschränkung der Eiweißzufuhr,
- die Behandlung einer aktuell auftretenden Anämie,
- die Beendigung des Rauchens
- die Optimierung der Blutzuckereinstellung.
Nierenschädigende Substanzen wie Röntgenkontrastmittel, nicht-steroidale Antirheumatika z.B. Voltaren®, Ibuprofen® sollten möglichst gemieden werden. Darüber hinaus gilt natürlich weiterhin ganz wichtig:
- eine Gewichtsreduktion,
- eine Ernährungsumstellung (weniger, aber hochwertiges Eiweiß),
- die Reduktion von Kochsalz (vor allem wegen des Bluthochdrucks),
- die Reduktion des Alkoholkonsums,
- und regelmäßige körperliche Aktivität
- sowie eine optimale Blutdruck- und Blutzuckereinstellung (HbA1c 6,5-7,5% bzw. 48-58mmol/molHb).
- frischem Harnwegsinfekt
- während der Regelblutung
- bei hohem Fieber
- bei entgleistem Blutzucker
- bei entgleistem Blutdruck
- Stress, z.B. Operationen
- Körperliche Aktivität
Medikamente zur Verbesserung der Nierenfunktion bzw. solche, die bei Niereninsuffizienz zu berücksichtigen sind
Medikamente des so genannten "Renin-Angiotensin-Aldosteronsystems" stehen im Vordergrund. Dies sind Medikamente, die an der Nebenniere und in den Wasserhaushalt eingreifen z.B. ACE-Hemmer, AT-1-Rezeptorblocker, oft kombiniert mit einer mäßigen Entwässerung. In diesem Zusammenhang haben sich auch die neueren Antidiabetika der Gruppe der SGLT-2-Hemmer als sehr vorteilhaft erwiesen, da sie ein Voranschreiten eines diabetischen Nierenschadens verlangsamen oder reduzieren. Sie sind daher auch entsprechend der neuen Leitlinien nicht nur bei Herzschwäche und Erkrankungen der Herzkranzarterien an erster Stelle zu nennen, sondern auch im Zusammenhang mit einem diabetischen Nierenschaden. Bei Menschen mit Typ 2 Diabetes sollte man unbedingt auch die Hyperlipidämie reduzieren und das LDL- Cholesterin auf unter 100mg/dl senken – sind bereits Gefäßschäden vorhanden sogar auf unter 70mg/dl!
Eine Blutdruckeinstellung auf unter 140/90mmHg gilt für alle Patienten mit Diabetes (ADA= American Diabetes Assoziation). Für Patienten mit bereits vorhandener Mikroalbuminurie sogar < 130/80mmHg (ADA-Empfehlung). Die klassischen Diabetes-Medikamente wie auch z.B. Metformin können weiterhin auch bei einer leichten Niereninsuffizienz in reduzierter Dosis, eingenommen werden. Ebenso sind DPP-4-Hemmer in reduzierter Dosis, einzelne Substanzen auch bei schwerer Niereninsuffizienz verordnungsfähig (Sitagliptin 25mg). GLP-1-Rezeptorantagonisten, die vor allem bei massivem Übergewicht eingesetzt werden, können ebenfalls je nach Präparat auch bei mittelgradiger Niereninsuffizienz eingesetzt werden (Liraglutide/Semaglutide). Die zuvor schon angesprochenen SGLT-2-Hemmer reduzieren Herz-Kreislauf-Endpunkte wie Herzinfarkt und Schlaganfall, aber auch das Risiko für eine Niereninsuffizienz. Das Risiko für Infektionen im Bereich des Genitale aber auch eine mögliche Ketoazidose muss besprochen werden.
Insulin ist bei allen Formen eines chronischen Nierenschadens das Mittel der Wahl, da es optimal steuerbar ist. Die Dosis muss der Niereninsuffizienz entsprechend oft angepasst, meist reduziert werden. Deshalb sollte trotz allen Fortschritts der letzten Jahre rechtzeitig bei eingeschränkter Nierenfunktion auf eine Insulinbehandlung umgestellt werden. Ein Nephrologe sollte wegen der Frage einer anstehenden Nierenersatztherapie einbezogen werden. Der HbA1c-Wert ist bei niereninsuffizienten Menschen mit Diabetes oft erniedrigt. Dies hat z.T. mit der kürzeren Lebensdauer der Erythrozyten zu tun.
Die Mehrheit aller Menschen mit Diabetes die eine Nierenersatztherapie benötigen sind an Typ-2 Diabetes erkrankt – aber auch an Typ 1 Diabetes. Frauen haben laut Weltnierentag (9.3. 23 diabetes DE) häufiger Risikofaktoren, für die Entstehung einer diabetischen Nephropathie als diabetische Männer (amerikanische Untersuchung von 2020 Mayo Clinic, Proc 2020;95). Diese sind:
- Hypertonie
- Hyperglykämie
- Adipositas
- Hyperlipidämie.
Frauen haben auch eine höhere Sterblichkeitsrate. Insbesondere die Hyperglykämie in Kombination mit der Hypertonie scheinen die kleinen Blutgefäße der Nieren besonders zu schädigen (Haak Th. 3/23) – die Prävention und jährliche Kontrollen der Mikroalbuminurie scheinen wegweisend, um ein Fortschreiten der Niereninsuffizienz zu vermeiden. Ein optimaler Lebensstil und kombiniert oft eine medikamentöse Therapie scheinen der Schlüssel zu sein.
Die diabetische Retinopathie
Die diabetische Retinopathie und die Makulopathie sind neben der Nephropathie die häufigsten mikrovaskulären Komplikationen des Diabetes. Die Veränderungen werden anfänglich von den Betroffenen oft nicht bemerkt, Frühformen der diabetischen Retinopathie verursachen keine Minderung der Sehstärke. Nur aufwendige Tests, die in der Routine nicht durchgeführt werden, zeigen beginnende Veränderungen an den Nervenzellen, die am "Sehen" beteiligt sind (Hammes, H.P, Lemmen, K.D.- Gesundheitsbericht 2017).
Also: Nur durch regelmäßige Untersuchungen können Frühformen der diabetischen Retinopathie entdeckt werden (Hannes, Lemmen, Gesundheitsbericht 2022, z.B. optische Kohärenztomographie= OCT).

Einige Neuerungen sind allerdings in den Leitlinien zur diabetischen Retinopathie aktuell zu berücksichtigen: Wenn ein Patient mit Diabetes bisher keinerlei Hinweise auf eine Retinopathie hatte, dazu auch keine weiteren Erkrankungen wie eine Hypertonie oder pathologische Nierenveränderungen und einen guten HbA1c-Wert (<7%), dann reicht ein Screening-Intervall von 2 Jahren aus. Ansonsten bleibt es bei den Empfehlungen zur jährlichen Kontrolle beim Augenarzt aus den oben angeführten Gründen.
In Deutschland fehlen große Studien, die ein genaueres Risiko für die Wahrscheinlichkeit des Auftretens einer diabetischen Retinopathie abschätzen lassen.
Zwei Studien geben jedoch Hinweise für die zu erwartende Häufigkeit. In der Gutenbergstudie (1124 Patienten mit Diabetes von insgesamt 15.010 untersuchten Menschen, Mainz) betrug die Häufigkeit der Retinopathie – nicht unterschieden nach Typ 1- oder Typ 2 Diabetes etwa 22% (= Jeder 5.war betroffen!).
In der DPV-Studie (mit insgesamt 64.700 Menschen mit Typ 2 Diabetes) hatten etwa 20% nach 9 Jahren Diabetesdauer und einem HbA1c-Wert von im Mittel 6,1% eine diabetische Retinopathie. Etwa - 9% eine fortgeschrittene Retinopathie – 0,8% eine Maculopathie. Neuere Daten großer Krankenkassen zeigen allerdings, dass bei der Neudiagnose eines Typ 2 Diabetes nur bei 30% eine Augenuntersuchung erfolgt!
Da aber ca. 30-40% der Menschen mit Typ 2 Diabetes bereits zu Beginn ihrer Erkrankung eine "milde Retinopathie" haben und sich bei Menschen mit Diabetes und Retinopathie das Risiko für Herz-Kreislauferkrankungen verdoppelt, ist ein rechtzeitiges Erkennen unabdinglich!
Eine rückläufige Tendenz zur diabetischen Retinopathie bei Kindern und Jugendlichen scheint auf die verbesserte glykämische Kontrolle durch die neueren Diabetestechnologien zurückzuführen zu sein. (Professor R Holl 1/23 DDG Redaktion). Lange Zeit war wohl die diabetische Retinopathie eine der Hauptkomplikationen bei Kindern und Jugendlichen mit Typ 1 Diabetes (Pediatric Diabetes Journal).
Retinopathieerkrankungen sind weltweit rückläufig, aber in Deutschland wird – wie weltweit – der Behandlung der Hypertonie zu wenig Beachtung geschenkt (Holl 23, Hannes). Die Augen sind der Spiegel für den allgemeinen Gefäßzustand – Präventionsmaßnahmen an diesem Organ sind insbesondere bei einem Diabetes essentiell (Hannes, Mannheim 23).

Pathogenese der Retinopathie
Durch Hyperglykämie kommt es zu Einlagerungen von Eiweißen und fettähnlichen Substanzen in die Blutgefäße der Netzhaut mit der Ausbildung von Mikroaneurysmen, aus denen auch Blut austreten und sich dann "harte Exsudate" (aus Fettablagerungen!) bilden können, die zur "nicht proliferativen Retinopathie" führen.
Durch Gefäßneubildungen (= proliferative Retinopathie = brüchige Gefäßwände) verschlechtert sich paradoxerweise sogar die Durchblutung der Netzhaut – Blutungen können auftreten und Gefäße wachsen in den Glaskörper ein. Ein weiterer wichtiger Risikofaktor neben einem zu hohen Blutzucker ist ein erhöhter Blutdruck (Hypertonie) sowie auch das Rauchen!
Allgemeine Therapiemaßnahmen bei diabetischer Retinopathie
- Gute Einstellung des Blutzuckers (eine nicht zu schnelle Senkung des Blutzuckers beim Typ-1-Diabetiker, dies könnte sogar zu einer Verschlechterung der Retinopathie führen = early worsening)
- Blutdrucknormalisierung (z.B. ACE-Hemmer, AT1 Blocker)
- Nicht mehr rauchen, besonders Typ 1 Diabetiker
- Behandlung der Hypercholesterinämie (LDL-Cholesterin)
Therapie bei fortgeschrittenen Stadien
Bei proliferativer diabetischer Retinopathie /Makulopathie ist die Laserfotokoagulation der Goldstandard, aber auch die Injektion von Wachstumsfaktoren-Hemmern (Avastin®, Lucentis®, Eylea®= VEGT-Antikörper) werden von spezialisierten Augenärzten in oft mehreren Sitzungen direkt in das Auge injiziert, in einigen Fällen auch Steroide (z.B. Cortison). Bei drohender Netzhautablösung auch die Vitrektomie: wenn eine Entfernung von Blutungen bzw. – Neubildungen im Glaskörper nicht gelingt, kann dieser auch komplett entfernt werden – so wird versucht die Netzhaut ggf. wieder an die sie ernährende Aderhaut anzulegen!
Fazit
Die mikroangiopathischen Komplikationen bei Menschen mit Diabetes würden ihren Schrecken verlieren, wenn sie frühzeitiger entdeckt und dann konsequent behandelt würden.
Eine frühzeitige Diagnostik in Form von Screening-Untersuchungen wurden denn auch von den Fachgesellschaften schon seit langem immer wieder gefordert – es ist nicht nachvollziehbar aus menschlichen, wie auch ökonomischen Gründen, warum diese Forderung nicht konsequent und rasch umgesetzt wird.
|
|
Erschienen in: Diabetes-Forum, 2023; 35 (7/8) Seite 22-27


