Seit Jahren sind Systeme zur kontinuierlichen Glukosemessung (CGM) bei Menschen mit Diabetes, insbesondere Typ 1, sehr weit verbreitet und finden Einsatz in Systemen zur automatisierten Insulindosierung. Trotz dieses Stellenwertes sind die Anforderungen an CGM-Systeme nur unzureichend reguliert, wobei jedoch die Messgenauigkeit der Systeme mittlerweile meist als ausreichend erachtet wird.
Um diese Lücke zu schließen, hat die Scientific Division der International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) die Arbeitsgruppe CGM gegründet (WG-CGM; https://ifcc.org/ifcc-scientific-division/sd-working-groups/wg-cgm/), deren Leiter von 2019 bis 2024 Dr. Guido Freckmann vom Institut für Diabetes-Technologie in Ulm (IfDT) war, und die seit 2025 von Dr. Stefan Pleus, ebenfalls vom IfDT, geleitet wird.
Die IfDT-CGM-Studie
Zur Unterstützung der WG-CGM hat das IfDT in Eigenregie und zu einem erheblichen Teil selbstfinanziert eine Studie durchgeführt. Finanziell oder mit Material unterstützt haben: Ascensia Diabetes Care Holdings AG, BIONIME Corporation, Diabetes Center Berne, i-SENS, Inc. und Roche Diabetes Care GmbH. Die ersten Ergebnisse wurden kürzlich veröffentlicht [Eichenlaub 2025, Link 2025]. Die Studie hatte zwei Ziele:
- Die Machbarkeit und Sicherheit der von der WG-CGM und weiteren Experten vorgeschlagenen Studienprozeduren [Eichenlaub 2024] sollte verifiziert werden.
- Die aktuellen CGM-Systeme der drei großen Hersteller sollten parallel auf ihre Leistung untersucht werden.
Es wurden Erwachsene mit Typ-1-Diabetes eingeschlossen, die über 15 Tage parallel je einen Sensor der CGM-Systeme FreeStyle Libre 3, Dexcom G7 und Medtronic Simplera trugen. An drei Tagen fanden häufige Vergleichsmessungen (alle 15 Minuten für 7 Stunden mit drei verschiedenen Vergleichsmessverfahren) mit gleichzeitiger Glukoseauslenkung statt. Ziel dieser Auslenkung war es, die Blutzuckerwerte unter ärztlicher Aufsicht gezielt mit schnellen Glukoseänderungsraten zuerst in den hyperglykämischen und dann in den hypoglykämischen Bereich zu bringen.
Mit der beschriebenen Prozedur zur Manipulation der Glukosewerte konnte der geforderte Mindestanteil von je 7,5 % innerhalb der kritischen Bereiche (Blutzuckerwerte < 70 und > 300 mg/dl, sowie schnell steigende und schnell fallende Werte, [Eichenlaub 2024]) erreicht werden [Link 2025].
Je nach betrachtetem Vergleichsmessverfahren unterschied sich die ermittelte Messgenauigkeit der CGM-Systeme (Tabelle 1) [Eichenlaub 2025]. Während FreeStyle Libre 3 und Dexcom G7 die höchste Übereinstimmung mit dem Laborgerät 1 zeigten, war dies bei Medtronic Simplera im Vergleich zu Laborgerät 2 der Fall. Insgesamt schnitten FreeStyle Libre 3 und Dexcom G7 etwas besser als Medtronic Simplera ab, welches eine deutliche, systematische negative Messabweichung gegenüber allen Vergleichsmessverfahren zeigte. Abbildung 1 veranschaulicht die Lage der CGM-Kurven und Vergleichsmessungen vor, bei und nach der induzierten Hyper- bzw. Hypoglykämie. Hier zeigte sich auch, dass Medtronic Simplera im niedrigen glykämischen Bereich eine bessere Übereinstimmung mit den Vergleichsmessungen aufwies.
 Tab. 1: Messgenauigkeit als mittlere absolute relative Differenz (MARD) der CGM-Systeme in Bezug auf verschiedene Vergleichsmessverfahren (bezogen auf den gesamten Messbereich).
Tab. 1: Messgenauigkeit als mittlere absolute relative Differenz (MARD) der CGM-Systeme in Bezug auf verschiedene Vergleichsmessverfahren (bezogen auf den gesamten Messbereich).
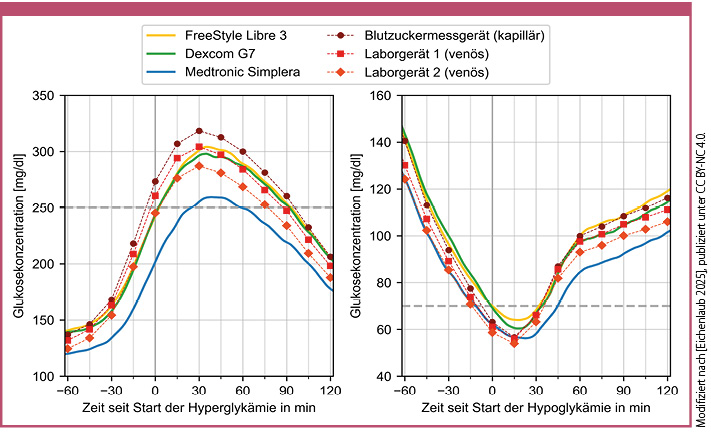 Abb. 1: Mittlerer Glukoseverlauf der CGM-Systeme und Vergleichsmessverfahren über alle Teilnehmer und Messtage während und um die Hyperglykämie (links) und während und um die Hypoglykämie. Für die linke Darstellung wurden die Kurven auf den Zeitpunkt des ersten Kapillarblutwertes > 250 mg/dl synchronisiert und für die rechte Darstellung auf den ersten Kapillarblutwert < 70 mg/dl.
Abb. 1: Mittlerer Glukoseverlauf der CGM-Systeme und Vergleichsmessverfahren über alle Teilnehmer und Messtage während und um die Hyperglykämie (links) und während und um die Hypoglykämie. Für die linke Darstellung wurden die Kurven auf den Zeitpunkt des ersten Kapillarblutwertes > 250 mg/dl synchronisiert und für die rechte Darstellung auf den ersten Kapillarblutwert < 70 mg/dl.
Bedeutung der Studie für die Standardisierung
Diese Studie zeigte, welchen Einfluss die Studienprozeduren und Vergleichsmessverfahren auf die Ergebnisse einer Performancebewertung haben können und warum sie deshalb standardisiert werden müssen.
Einfluss der Glukoseauslenkungsprozedur
In der Studie wurde eine Glukoseauslenkungsprozedur gewählt, die die CGM-Systeme deutlich mehr herausfordert als beispielweise die Prozeduren in den Zulassungsstudien der Hersteller. Aus diesem Grund ist die mittlere absolute relative Differenz (MARD) der Systeme deutlich höher als von den Herstellern berichtet [Alva 2023, Garg 2022]. Sie stellt jedoch sicher, dass alle relevanten glykämischen Situationen (Glukosewerte und -änderungsraten), die im Alltag von Menschen mit Diabetes vorkommen, abgedeckt sind [Eichenlaub 2024].
Standard für Vergleichsmessverfahren
Die Messgenauigkeit wird nicht absolut, sondern immer in Bezug auf ein Vergleichsmessverfahren ermittelt. Dabei wird davon ausgegangen, dass dieses Vergleichsmessverfahren "richtig" ist, also keinen oder nur einen vernachlässigbaren Messfehler aufweist. In diesem Fall müssten die CGM-Systeme gegen alle Vergleichsmessverfahren gleich abschneiden, was, wie diese Studie zeigt, nicht der Fall ist. Es müssen also Kriterien für die Genauigkeit der Vergleichsmessverfahren definiert werden [Pleus 2024]. Dazu kommt, dass die interstitielle Flüssigkeit, in der CGM-Systeme messen, nicht in ausreichenden Volumina entnommen werden kann, um damit Vergleichsmessungen durchzuführen. Deshalb muss eine alternative Probe genutzt werden. Hier wird meistens Kapillar- oder Venenblut verwendet. Die Studie zeigt jedoch unterschiedliche Ergebnisse für verschiedene Vergleichsproben, die größtenteils rein physiologisch bedingt sind [Pleus 2024]. Es muss also eine einheitliche Probe definiert werden [Freckmann 2021], die WG-CGM empfiehlt Kapillarblutproben [Freckmann 2025].
|
|
Erschienen in: Diabetes, Stoffwechsel und Herz, 2025; 34 (2) Seite 102-103


