Kontinuierliches Glukosemonitoring (CGM) stellt nicht nur eine der wichtigsten diagnostischen Optionen in der Diabetologie dar, sondern hat als rtCGM (real time CGM; CGM mit Anzeige der aktuellen Glukosewerte) die Diabetestherapie revolutioniert. Als Hilfsmittel für die Unterstützung und Erleichterung des Diabetesmanagements, besonders von Menschen mit Diabetes (MmD) mit Insulintherapie, ist rtCGM mittlerweile unverzichtbar.
Zusammenfassung
Mit der Einführung des kontinuierlichen Glukosemonitorings (CGM) im Jahr 1999 wurden neue Metriken zur Beurteilung der glykämischen Kontrolle eingeführt. Die CGM-Profile zeigten, dass nicht nur der Mittelwert der Glukosekonzentration relevant ist, der gut mit dem HbA1c-Wert korreliert, sondern auch Parameter, welche die Hyperglykämie, ganz besonders aber die Hypoglykämie und Glukosevariabilität, beschreiben. Diese hängen auf verschiedene Weise voneinander ab, sodass man sie komplex betrachten muss. Allerdings ist im klinischen Alltag die Zeit für umfassende Analysen begrenzt, sodass es sinnvoll erscheint, aus der Vielfalt der CGM-Daten einen einzigen Parameter zu kreieren, der ähnlich wie der HbA1c die Qualität der Einstellung beschreibt. Dazu müssten zusammengesetzte Metriken gefunden werden, die möglichst gut mit dem HbA1c-Wert korrelieren. Verschiedene zusammengesetzte Metriken wurden bisher entwickelt und publiziert. Sie weisen aber alle eine größere Komplexität auf. Welche Möglichkeiten es gibt, die Vielfalt an relevanten Parametern aus den CGM-Messungen in zusammengesetzten Metriken zu verbinden und zu einer die Einstellungsqualität beschreibenden Größe zusammenzufassen, wird nachfolgend beschrieben. Anschließend erfolgt die Berechnung von drei zusammengesetzten Metriken mit vorliegenden Daten aus einer nicht interventionellen, retrospektiven Querschnittsstudie des Klinikums Karlsburg. Deren gute Korrelation untereinander und mit dem HbA1c-Wert zeigt deren Eignung zur umfassenden glykämischen Beurteilung.
Schlüsselwörter
CGM, kontinuierliches Glukosemonitoring, glykämischer Status, Metriken
Comparison of CGM-based composite metrics for assessing glycaemic status in inpatient diabetes care
Summary
With the introduction of continuous glucose monitoring in 1999 new metrics for assessing glycemic control were also introduced. CGM profiles showed that not only the mean value of glucose concentration is relevant, which also correlates well with the HbA1c value. Parameters that describe hyperglycemia, but especially hypoglycemia and glucose variability, are also relevant. These depend on each other in various ways, so they must be considered in a complex manner. However, in everyday clinical practice, the time available for comprehensive analyses is limited, so it seems sensible to create a single parameter that describes glycemia as comprehensively as possible. To do this, composite metrics would have to be found that correlate as closely as possible with the HbA1c value. Various composite metrics have already been published. However, they are all quite complex. The possibilities of combining the variety of relevant parameters from the CGM measurements in composite metrics and combining them into a variable that describes the quality of the settings are described below. Three composite metrics are calculated below using data from a non-interventional, retrospective cross-sectional study conducted at Karlsburg Hospital. Their good correlation with each other and with the HbA1c value demonstrates their suitability for comprehensive glycemic assessment, including the risk for the development of diabetic secondary diseases.
Keywords
CGM, continuous glucose monitoring, glycemic status, metrics
Einleitung
Durch fortlaufend mögliche Einblicke in die Dynamik der Glukoseregulation wird es MmD ermöglicht, proaktiv auf den Verlauf der Glukosekonzentration Einfluss zu nehmen [Thomas 2023a]. Sie können durch Nutzung der Trendinformation Hypo- und Hyperglykämien weitgehend vermeiden. Individualisierbare Alarmfunktionen unterstützen sie dabei [Heinemann 2018, van Beers 2016]. In Verbindung mit entsprechenden smarten Insulinpens, also Pens mit Hilfs- und Erinnerungsfunktionen, unterstützt CGM die korrekte Durchführung des Insulinmanagements und erinnert an Bolusinjektionen [Bailey 2017]. Darüber hinaus stellt rtCGM den notwendigen Systempartner für die Steuerung der automatisierten Insulinabgabe (automated insulin delivery, AID) in AID-Systemen dar [Bassi 2023, Thomas 2023b].
Aus den quasi lückenlos verfügbaren Glukosewerten lassen sich auch Parameter ableiten, die vor dem Einsatz von CGM nur schwer verifizierbar waren. Dies betrifft zum Beispiel die Anteile der Zeit in verschiedenen Glukosebereichen, die Zeit im Zielbereich (Time in Range, %TIR), die Zeit unterhalb (Time below Range, %TBR) und oberhalb des Zielbereichs (Time above Range, %TAR) [Rodbard 2020]. Diese helfen bei der Beurteilung der Güte der Glukosekontrolle. Weiterhin ergeben sich für MmD und die Diabetesteams konkrete Ansatzpunkte für die Optimierung der Diabetestherapie, falls dies notwendig erscheint. Die Darstellung der Glukosedaten erfolgt übersichtlich in den ambulanten Glukoseprofilen (AGPs) [Bergenstal 2013], wahlweise mit unterschiedlicher Farbgebung [Holt 2021]. Die genannten Parameter ergänzen den unabhängig von den CGM-Profilen gemessenen HbA1c. Deren Zielwerte zur Erreichung einer guten glykämischen Einstellung sind in einem internationalen Konsensus-Statement zu CGM festgelegt [Battelino 2019].
In der täglichen klinischen Routine ist es wichtig, dass anhand der vorliegenden glykämischen Parameter zeitnah auf die Glukosedynamik reagiert werden kann, was dann zu einer besseren Glukosekontrolle führt. Das war in der Vergangenheit nicht oder nur bedingt möglich anhand von punktuell mittels Blutzuckermessung erhaltener Daten.
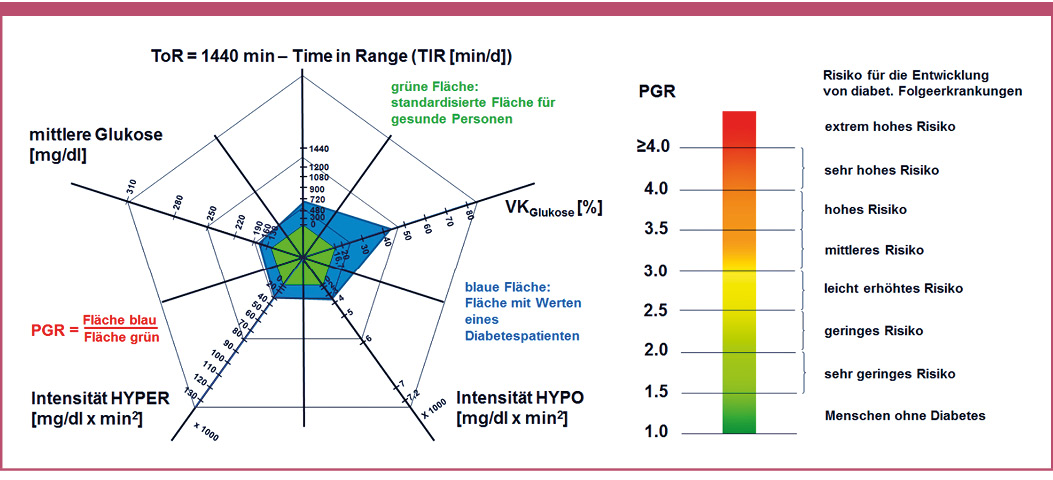 Abb. 1: Modell des Glukosepentagons. Die fünf Parameter, ermittelt aus den CGM-Daten eines MmD, spannen ein Fünfeck auf (blaue Fläche). Die grüne Fläche entspricht den Daten von stoffwechselgesunden Menschen. Der Quotient aus beiden Flächen ergibt einen dimensionslosen Parameter, den prognostischen glykämischen Risikoparameter (PGR). Dieser wurde aus einer großen Anzahl von Studien validiert in Bezug auf das Risiko für die Entwicklung von DFE (farbige Skala rechts) [Vigersky 2018].
Abb. 1: Modell des Glukosepentagons. Die fünf Parameter, ermittelt aus den CGM-Daten eines MmD, spannen ein Fünfeck auf (blaue Fläche). Die grüne Fläche entspricht den Daten von stoffwechselgesunden Menschen. Der Quotient aus beiden Flächen ergibt einen dimensionslosen Parameter, den prognostischen glykämischen Risikoparameter (PGR). Dieser wurde aus einer großen Anzahl von Studien validiert in Bezug auf das Risiko für die Entwicklung von DFE (farbige Skala rechts) [Vigersky 2018].
Unabhängig davon hatte sich die Messung des Surrogatparameters HbA1c etabliert, für welchen die grundlegenden Studien "Diabetes Control and Complications Trial (DCCT)" [DCCT Research Group 1995] für Menschen mit Typ-1-Diabetes (MmT1D) und "United Kingdom Prospective Diabetes Study (UKPDS)" [Stratton 2000] für Menschen mit Typ-2-Diabetes (MmT2D) den Zusammenhang zwischen dem HbA1c und dem Risiko für die Entwicklung von diabetischen Folgeerkrankungen (DFE) gezeigt hatten. Folglich ergab sich das Bestreben, Daten aus den CGM-Messungen möglichst auf den gut etablierten HbA1c umzurechnen. Beispielsweise zeigte eine Analyse von ausgewählte HbA1c- und %TIR-Datenpaaren aus 18 publizierten Untersuchungen, dass die Umrechnung von %TIR-Werten in HbA1c-Werte kritisch zu bewerten ist [Vigersky 2019]. Obwohl die Datenpaare gut miteinander korrelierten, lässt sich feststellen, dass innerhalb des angegebenen 95 %igen Konfidenzintervalls bei dem Rückschluss von %TIR-Werten auf den HbA1c und umgekehrt eine erhebliche Datenbandbreite entsteht. Bei Annahme einer %TIR von 50 % können die HbA1c-Werte zwischen 7,95 % und 8,55 % liegen. Umgekehrt liegt die %TIR bei Annahme eines HbA1c-Wertes von 8,2 % zwischen 47 % und 54 %. Die Abweichungen betreffen den gesamten Bereich der Datenpaare, der als linear angenommen wurde. Die Abweichungen sind damit größer als ein Wert, den man als Erfolg im Rahmen einer therapeutischen Intervention bewertet.
Es stellt sich die Frage, ob man von der mit CGM ermittelten %TIR wirklich zuverlässig auf den HbA1c-Wert schließen kann, um darauf basierend das Risiko zur Entwicklung von DFE anzugeben. Dagegen ist die Korrelation mit der mittleren Glukosekonzentration höher. Daraus lässt sich ein geschätzter HbA1c-Wert berechnen, ursprünglich bezeichnet als eHbA1c und später modifiziert in den sogenannten Glukose-Management-Indikator (GMI) [Bergenstal 2018]. Die Formel zu dessen Berechnung lautet: GMI (%) = MSG (mg/dl) x 0,02392 + 3,31 (1) bzw.GMI (%) = MSG (mmol/l) x 0,43056 + 3,31 (2) mit: MSG = mittlere Sensorglukose
Allerdings zeigten Analysen von großen Patientenkohorten, dass eine nichtlineare Diskordanz zwischen dem GMI und dem HbA1c besteht [Dunn 2022]. Zu beachten ist auch, dass die Rückführung auf den HbA1c-Wert, egal von welchem Parameter aus dies geschieht, nur einen Teil der Glukosehomöostase abbildet. Akute Schwankungen der Glukosekonzentrationen, d. h. die Glukosevariabilität, werden durch den HbA1c nicht gekennzeichnet. Wird dies aus dem Mittelwert der Glukosekonzentration (also dem GMI) geschlussfolgert bzw. auch aus der TIR, so bleiben z. B. Hypoglykämien unberücksichtigt. Im Grunde genommen sind weder gemessene HbA1c-Werte, noch einzelnen Parameter wie die %TIR in der Lage die Langzeitprognose von MmD mit hoher Sicherheit anzugeben, für die Abschätzung der Wahrscheinlichkeit allerdings schon. Trotzdem stellt sich die Frage, ob aus der Datenfülle, die beim CGM entsteht, eine genauere Prognose für die Entwicklung von DFE ableitbar ist. Zusammengesetzte Metriken könnten dabei hilfreich sein.
 Abb. 2: Beispiel für die Darstellung der erfolgreichen Stoffwechseloptimierung über 8 Tage bei einem MmT1D. An der Größe der Flächen des Glukosepentagons ist unmittelbar der therapeutische Erfolg sichtbar (oben links: mittleres Glukosepentagon über die gesamte Zeit; oben Mitte: Vergleich der Pentagramme an zwei verschiedenen ausgewählten Tagen (Tag 6 vs. Tag 1); oben rechts: Vergleich der Flächenwerte – und damit des PGR – über die Tage des betrachteten Zeitraumes). rot: MmT1D; grün: Fläche eines stoffwechselgesunden Menschen; unten: Darstellung der einzelnen Tage [Rama Chandran 2020].
Abb. 2: Beispiel für die Darstellung der erfolgreichen Stoffwechseloptimierung über 8 Tage bei einem MmT1D. An der Größe der Flächen des Glukosepentagons ist unmittelbar der therapeutische Erfolg sichtbar (oben links: mittleres Glukosepentagon über die gesamte Zeit; oben Mitte: Vergleich der Pentagramme an zwei verschiedenen ausgewählten Tagen (Tag 6 vs. Tag 1); oben rechts: Vergleich der Flächenwerte – und damit des PGR – über die Tage des betrachteten Zeitraumes). rot: MmT1D; grün: Fläche eines stoffwechselgesunden Menschen; unten: Darstellung der einzelnen Tage [Rama Chandran 2020].
Zu diesem Zweck werden nachfolgend drei publizierte Metriken betrachtet: der Q-Score [Augstein 2015], das erweiterte Glukosepentagonmodell (Comprehensive Glucose Pentagon, CGP) [Vigersky 2018, Thomas 2018] und der glykämische Risikoindex (Glycemia Risk Index, GRI) [Klonoff 2023]. Sie enthalten alle einen zusammenfassenden Parameter als eine einzelne Zahl. Es lassen sich aber auch Details über die glykämische Regulation ableiten, so beim Glukosepentagon. Ziel der Analyse ist es, anhand von klinischen Daten von Patienten mit Diabetes, die im Klinikum Karlsburg betreut wurden, den jeweils für die Beurteilung der Diabetesprognose wichtigen Parameter für die drei zusammengesetzten Metriken zu berechnen. Weiterhin sollte untersucht werden, ob die Parameter der drei Metriken miteinander korrelieren und welcher mathematische Zusammenhang sich dabei ergibt.
AID: Automated Insulin Delivery (automatische Insulindosierung)
CGM: Continuous Glucose Monitoring (kontinuierliches Glukosemonitoring)
CGP: Comprehensive Glucose Pentagon (umfassendes Glukosepentagon)
DCCT: Diabetes Control and Complications Trial
DFE: diabetische Folgeerkrankungen
GMI: Glukose-Management-Indikator
GRI: Glycaemia Risk Index (glykämischer Risikoindex)
iscCGM: CGM mit intermittierendem Scannen
MmD: Menschen mit Diabetes
MmT1D: Menschen mit Typ-1-Diabetes
MmT2D: Menschen mit Typ-2-Diabetes
MODD: mittlere Sensorglukose (entspricht der mittleren Glukosekonzentration, gemessen mit CGM)
MSG: Standardabweichung
PGR: prognostischer glykämischer Risikoparameterrt
CGM: real time CGM (CGM mit Anzeige der aktuellen Glukosewerte)
SMBG: Selbstmessung der Blutglukose
%TAR: Time above Range (prozentualer Anteil der Zeit über dem Zielbereich), > 10,0 mmol/l (> 180 mg/dl)
%TBR: Time below Range (prozentualer Anteil der Zeit unter dem Zielbereich) < 3,9 mmol/l (< 70 mg/dl)
%TIR: (prozentualer Anteil der Zeit im Zielbereich) 3,9 – 10,0 mmol/l (70 – 180 mg/dl)
UKPDS: United Kingdom Prospective Diabetes Study
Zusammengesetzte Metriken
Die sich aus CGM-Messungen ergebende %TIR wird auch in internationalen Standards als Parameter zur Beurteilung der glykämischen Kontrolle empfohlen [Battelino 2019, Danne 2017]. Allerdings reagiert die %TIR nicht ausreichend empfindlich auf Hypoglykämien, was ihre Bedeutung als alleinige Metrik zur Beurteilung der Glykämie einschränkt. Zusammengesetzte Metriken aus mehreren Parametern sind deshalb sinnvoll. Schließlich ergeben sich aus CGM-Messungen entsprechend dem internationalen Konsensus-Statement sieben relevante Größen [Battelino 2019]:
- die mittlere Glukosekonzentration und daraus abgeleitet der GMI
- der Variationskoeffizient (CV) (Standardabweichung/mittlere Glukose x 100 %)
- die prozentualen Anteile der Zeit:
- oim Glukosezielbereich (%TIR) von 70 – 180 mg/dl (3,9 – 10,0 mmol/l)
- oim hypoglykämischen Bereich (%TBR Stufe 1) von 54 – < 70 mg/dl (3,0 – < 3,9 mmol/l)
- oim sehr niedrigen hypoglykämischen Bereich (%TBR Stufe 2) < 54 mg/dl (< 3,0 mmol/l)
- oim hyperglykämischen Bereich (%TAR Stufe 1) von > 180 – 250 mg/dl (> 10,0 – 13,9 mmol/l)
- oim hohen hyperglykämischen Bereich (%TAR Stufe 2) von > 250 mg/dl (> 13,9 mmol/l)
Zwischen diesen bestehen zum Teil Zusammenhänge. Daraus folgt, dass die Verbesserung eines Parameters im Sinne einer besseren glykämischen Kontrolle andere Parameter beeinflussen kann, was für einen solchen ggf. auch negativ sein kann, falls dieser allein betrachtet wird. Zum Beispiel kann eine Verringerung der Werte im hypoglykämischen Bereich (%TBR) eine Erhöhung des Mittelwertes der Glukosekonzentration zur Folge haben, damit auch des GMI und bei entsprechender Messung des HbA1c. Weiterhin lassen sich aus den primär in den CGM-Auswertungen ablesbaren Daten abgewandelte Größen errechnen, wie zum Beispiel die Variabilität zwischen den gemessenen Tagen (MODD, Mean of Daily Differences [Rodbard 2020, Rodbard 2009]) oder der durchschnittliche tägliche Risikobereich (average daily risk range, ADRR; umfasst LBGI und HBGI, das sind die niedrigen (L) und hohen (H) Glukoseindizes [Kovatchev 2006]). Aus diesen Parametern lassen sich Ableitungen für eine Optimierung der Therapie finden. Eine andere Frage ist jedoch, ob sich aus der Anzahl der Parameter ableiten lässt, wie die Prognose für die Entwicklung von DFE aussieht. Folglich ist es wichtig, zusammengesetzte Metriken zu entwickeln, die möglichst umfassend die Glykämie beschreiben und das nach Möglichkeit mit einem einzigen, aus den einzelnen Parametern errechneten Wert. Solche Metriken sollten gewichtet die Daten der einzelnen Glukosebereiche, die Glukosevariabilität, den Mittelwert der Glukosekonzentration usw. enthalten.
 Tab. 1: Ausgangsmerkmale/Baselinedaten der Teilnehmer.
Tab. 1: Ausgangsmerkmale/Baselinedaten der Teilnehmer.
Eine solche Metrik ist der Q-Score [Augstein 2015]. Dieser setzt sich aus fünf Parametern zusammen: dem Mittelwert der Glukose (MG), der Glukosevariabilität an einem Tag (Range), der Zeit im hyperglykämischen Bereich über 10,0 mmol/l (180 mg/dl; t> 10,0), der Zeit im hypoglykämischen Bereich unter 3,9 mmol/l (70 mg/dl; t< 3,9) und der Variabilität zwischen den gemessenen Tagen (MODD). Deren Summe ergibt einen dimensionslosen Bewertungsfaktor, der zu einer Konstante hinzugezählt wird: Q-Score = 8 + (MSG – 7,8)/1,7 + (Range – 7,5)/2,9 + (t< 3,9 – 0,6)/1,2 + (t> 10,0 – 3,9)/4,8 + (MODD* – 1,8)/0,9 (3)
(1)Die genannten Beziehungen beziehen sich auf Glukosewerte in der Maßeinheit mmol/l. Liegen mg/dl vor, so müssen diese zuerst umgerechnet werden. Damit erfasst der Q-Score verschiedene glykämische Parameter in einem Wert.
Der sich ergebende dimensionslose Wert für den Q-Score ist Ausdruck für die Güte des Stoffwechsels:
- < 4,0 = exzellent, nahe normoglykämischer Stoffwechselqualität
- 4,0 bis < 7,0 = sehr gute Stoffwechselqualität
- 7,0 bis < 10,0 = gute Stoffwechselqualität
- 10 bis < 14,0 = moderate Stoffwechselqualität
- 14 bis < 18,0 = schlechte Stoffwechselqualität
- > 18 = sehr schlechte Stoffwechselqualität
Auf dieser Grundlage ergibt sich aus den CGM-Daten eine Risikostratifizierung in Bezug auf die Güte des Stoffwechsels. Dies erfolgt mittels Vergleich mit parallel dazu vorliegenden HbA1c-Werten [Augstein 2025].
Der Q-Score bietet dem Arzt die Möglichkeit zusätzlich zum HbA1c das allgemeine Diabetesmanagement schnell zu beurteilen und Empfehlungen auf Grundlage der Punktzahl abzugeben. Im Gegensatz zum HbA1c sind in dem Q-Score aber Parameter enthalten, wie die Glukosevariabilität über konsekutive Tage und die Zeit im hypoglykämischen und hyperglykämischen Bereich.
Eine weitere zusammengesetzte Metrik ist der glykämische Risikoindex (GRI) [Klonoff 2023]. Dieser gewichtet die prozentualen Anteile der Zeit außerhalb des Glukosezielbereichs, entsprechend: GRI = (3,0 × VLow) + (2,4 × Low) + (1,6 × VHigh) + (0,8 × High) (4) mit: VLow = very low-glucose hypoglycemia (prozentualer Anteil der Zeit < 54 mg/dl bzw. < 3,0 mmol/l), Low = low-glucose hypoglycemia (prozentualer Anteil der Zeit 54 – < 70 mg/dl bzw. 3,0 – < 3,9 mmol/l), VHigh = very high-glucose hyperglycemia (prozentualer Anteil der Zeit > 250 mg/dl bzw. > 13,9 mmol/l), High = high-glucose hyperglycemia (prozentualer Anteil der Zeit > 180 – 250 mg/dl bzw. > 10,0 – 13,9 mmol/l)
Ein wesentlicher Vorteil dieser Metrik ist, dass die für die Berechnung des GRI notwendigen Größen direkt aus den mit CGM-gemessenen Daten und in der Software ausgewiesenen Daten ablesbar sind, also nicht erst Berechnungen durchgeführt werden müssen, wie z. B. bei der MODD beim Q-Score. Nachteilig ist, dass kein Zugang zum Risiko für die Entwicklung von DFE besteht, was ja ein wichtiger Aspekt bei der Beurteilung des HbA1c-Wertes ist. Bezüglich des GRI ist bisher keine Validierung in diese Richtung bekannt.
Eine weitere zusammengesetzte Metrik stellt das erweiterte Glukosepentagonmodell (CGP) dar [Vigersky 2018, Thomas 2018]. Das CGP-Modell umfasst fünf Parameter, entsprechend für die fünf Achsen eines Pentagons.
Dies sind:
- die mittlere Glukosekonzentration
- der Variationskoeffizient (CV) (Standardabweichung/mittlere Glukose x 100 %)
- die Intensität von Hypoglykämien
- die Intensität von Hyperglykämien
- die "Time outside of Range", also die Gesamtzeit eines Tages (1440 min) minus der Time in Range (%TIR)
Die Intensitäten von Hypoglykämien und Hyperglykämien ergeben sich aus dem Vektorprodukt von den Flächen unter der Kurve pro Tag und der Zeit pro Tag im hypo- bzw. hyperglykämischen Bereich. Das Pentagon mit den Daten eines MmD spannt eine fünfeckige Fläche auf (blaue Fläche in Abbildung 1). Diese wird ins Verhältnis gesetzt mit der Fläche, die sich für einen Menschen ohne Diabetes ergibt (grüne Fläche in Abbildung 1). Aus der Division beider Flächeninhalte ergibt sich ein dimensionsloser Faktor, benannt als prognostischer glykämischer Risikoparameter (PGR). Damit entsteht aus den fünf Parametern ein dimensionsloser Parameter, vergleichbar mit dem HbA1c oder dem GMI. Allerdings beinhaltet er nicht nur die gemittelte Glykämie, sondern auch Hypoglykämien und deren Auswirkung, z. B. auf die Vergrößerung des Variationskoeffizienten. Der PGR wurde anhand verschiedener Studien evaluiert, in denen Bezug auf die Entwicklung von DFE genommen wurde. Daraus ergab sich die Einordnung des PGR in Bezug auf das Risiko für langfristige diabetische Komplikationen.
 Tab. 2: Korrelation zwischen Parametern für die kurzfristige glykämische Kontrolle (MSG = mittlere Sensorglukose).
Tab. 2: Korrelation zwischen Parametern für die kurzfristige glykämische Kontrolle (MSG = mittlere Sensorglukose).
Neben dem dieses Risiko beschreibenden PGR lassen sich aus der Form der Fläche Rückschlüsse auf die Glukoseregulation ziehen. Beispielsweise bedeutet ein hoher Wert für die Intensität der Hypoglykämien, dass die Fläche und damit der PGR groß sind, obwohl vielleicht der Wert für die mittlere Glukosekonzentration gering ist (was bei der Messung des HbA1c-Wertes einen niedrigen, ein geringes Risiko für DFE vortäuschenden Wert ergeben würde). Auch treten im Zusammenhang mit einer großen Intensität von Hypoglykämien meist hohe Werte für den Variationskoeffizienten auf, was die Fläche ebenfalls vergrößert. Aus der Form der für den MmD zutreffenden Fläche lassen sich folglich auch Schlussfolgerungen über die glykämische Regulation ziehen, was einen Mehrwert darstellt gegenüber der alleinigen Einordnung des PGR als Parameter bzgl. der Entwicklung von DFE.
Schließlich ergibt sich aus der grafischen Darstellung noch der Vorteil, dass im Fall einer Stoffwechseloptimierung der therapeutische Erfolg an den Glukosepentagrammen unmittelbar sichtbar wird, insbesondere, wenn diese als tägliches Ergebnis aneinandergereiht werden (Abbildung 2) [Rama Chandran 2020].
Nachteilig ist bei dem Glukosepentagonmodell, dass sich ein Teil der Parameter nicht unmittelbar aus den Glukosedaten des ambulanten Glukoseprofils ableiten lässt. Das bedarf einer zusätzlichen Software, wie sie beispielsweise beim firmenunabhängigen "Nightscout Reporter" in 12 Sprachen verfügbar ist. Nightscout ist eine Open-Source-Cloud-Anwendung, die von MmD und Eltern von Kindern mit Diabetes genutzt wird, um ihre CGM-Daten zu visualisieren, zu speichern und zu teilen [Nightscout Reporter].
Mit dem glykämischen Risikoindex (GRI), dem Q-Score und dem prognostischen glykämischen Risikoparameter (PGR) aus dem Glukosepentagon wurden drei Metriken entwickelt, welche verschiedene relevante Glukosedaten zu einem integralen Parameter zusammensetzen und damit einen schnellen Überblick über die Qualität der Stoffwechseleinstellung ermöglichen. Dieser integrale Parameter hat eine Bedeutung ähnlich des HbA1c-Wertes, allerdings mit mehr integrierten Daten wie Hypoglykämien und Glukosevariabilität, welche ebenfalls die Glykämie bestimmen. Obwohl sich also aus den zusammengesetzten Metriken viele Details ablesen lassen, bietet die sich ergebende einzige Zahl die Möglichkeit der sofortigen klinischen Bewertung eines speziellen Patienten allein aus CGM-Daten heraus [Nguyen 2020]. Beim Glukosepentagon wurde der integrale Parameter zusätzlich bezüglich der Entwicklung von diabetischen Folgeerkrankungen validiert. Auch wenn man für einen eindeutig gesicherten Zusammenhang eine Studie wie die DCCT bzw. die UKPDS unter Anwendung von CGM benötigen würde, was aus finanziellen Gründen aktuell schwer vorstellbar ist, so basiert die erfolgte Validierung auf einer Vielzahl bekannter Studien. Schließlich kann eine Vielzahl bekannter Faktoren auch den HbA1c-Wert verfälschen [Fath 2016]. So wird dieser nur anhand der erst nach sechs Stunden entstehenden stabilen Ketoamin-Phase beurteilt, wodurch Glukoseschwankungen praktisch nicht erfasst werden können. Die dem HbA1c innewohnenden Unbestimmtheiten lassen deshalb auch zu, dass andere Parameter in Bezug auf das Risiko der Entwicklung von diabetischen Folgeerkrankungen validiert werden, was die zusammengesetzten Metriken aus den CGM-Daten zusätzlich begründet.
 Abb. 3A-C: Streudiagramme von Daten aus iscCGM-Profilen für den GRI im Vergleich zum Q-Score (A), den Q-Score im Vergleich zum PGR des Glukosepentagons (B) und des GRI im Vergleich zum PGR des Glukosepentagons (C).
rote Werte: n = 155 MmT1D; blaue Werte: n = 106 MmT2D.
Abb. 3A-C: Streudiagramme von Daten aus iscCGM-Profilen für den GRI im Vergleich zum Q-Score (A), den Q-Score im Vergleich zum PGR des Glukosepentagons (B) und des GRI im Vergleich zum PGR des Glukosepentagons (C).
rote Werte: n = 155 MmT1D; blaue Werte: n = 106 MmT2D.
Validieren und Überführen der zusammengesetzten Metriken
Die zusammengesetzten Metriken umfassen unterschiedliche Parameter der glykämischen Regulation. Für den GRI werden die für dessen Berechnung notwendigen Parameter entsprechend Beziehung (4) in den Softwarelösungen unmittelbar ausgewiesen. Die Daten für die anderen beiden zusammengesetzten Metriken sind zwar nicht unmittelbar im AGP sichtbar, liegen aber innerhalb der Software vor. Damit lassen sich Korrelationen zwischen den drei zusammengesetzten Metriken herstellen. So ist der PGR aus dem Glukosepentagonmodell bezüglich des Risikos für die Entwicklung von diabetischen Folgeerkrankungen validiert. Die Korrelationen mit dem GRI und dem Q-Score würden ermöglichen, auch für diese Metriken dieses Risiko in einem einzelnen Wert anzugeben. Zur Vereinfachung wäre dazu eine Umrechnungsmatrix für die jeweiligen Größen (Q-Score, PGR, GRI, HbA1c) zu erstellen, wie Tabelle 3 zeigt.
 Tab. 3: Umrechnungsmatrix für den Q-Score mit weiteren Parametern der glykämischen Kontrolle. Anhand der Studienwerte für MmT1D und MmT2D sind die Werte für beide Diabetestypen gemittelt.
Tab. 3: Umrechnungsmatrix für den Q-Score mit weiteren Parametern der glykämischen Kontrolle. Anhand der Studienwerte für MmT1D und MmT2D sind die Werte für beide Diabetestypen gemittelt.
Beurteilung der Metriken mit Daten aus der stationären Diabetesversorgung
Um die zusammengesetzten Metriken zu vergleichen, wurden glykämische Daten von 155 MmT1D und 106 MmT2D aus der stationären Diabetesversorgung im Klinikum Karlsburg genutzt (Tabelle 1). Die Daten entstammen aus unter Alltagsbedingungen aufgezeichneten CGM-Profilen (aufgenommen mittels intermittierend gescannten CGM, iscCGM) einer nicht-interventionellen, retrospektiven Querschnittsstudie. Die Patientenrekrutierung war zwischen 2020 und 2023 vorgenommen worden.
Die CGM-Metriken %TIR, Glukose-Management-Indikator (GMI), Q-Score, GRI und des PGR aus dem Glukosepentagon (CGP) wurden miteinander korreliert. Der t-Test wurde beidseitig zum Vergleich zwischen den Diabetes-Typen verwendet.
Alle statistischen Analysen wurden mit PASW Statistics für Windows, Version 18.0 (SPSS Inc., Chicago, IL) durchgeführt. Die Ergebnisse werden als Mittelwerte ± Standardabweichungen (SD), Mediane (Interquartilsbereiche [IQR]) oder Prozentsätze (%) dargestellt. Für bivariate Vergleiche zwischen den Metriken wurden Streudiagramme erstellt und auf der Grundlage der linearen Regression die Pearson-Korrelationskoeffizienten berechnet. Für den nichtlinearen Parameter PGR des Glukosepentagons wurde die Spearman-Rangkorrelation angewendet.
Zur Untersuchung der Unterschiede zwischen Typ-1- und Typ-2-Diabetes wurde eine einseitige Varianzanalyse (analysis of variance, ANOVA) verwendet. Der Einfluss der glykämischen Qualität, der anhand des Q-Scores ermittelt wurde, wurde mittels zweiseitiger Varianzanalyse (zweiseitige ANOVA) untersucht.
Die Korrelationen zwischen den Parametern der einzelnen Metriken sind in Tabelle 2 zusammengestellt. Dabei zeigt sich eine enge Korrelation zwischen dem Q-Score, dem PGR aus dem Glukosepentagon und dem GRI. Diese zusammengesetzten Metriken bestehen aus eng verwandten Parametern für Hypo- und Hyperglykämie, mittlere Glukose und Glukosevariabilität, die für diese hohe Korrelation verantwortlich sind. Weiterhin zeigt sich die hohe Korrelation des HbA1c-Wertes mit der mittleren Glukosekonzentration, wogegen die Korrelation mit der %TAR geringer und der %TBR eher schwach ist. Das bestätigt, dass insbesondere Hypoglykämien zu berücksichtigen sind, was beim GMI und dem HbA1c nicht der Fall ist. Die Korrelation dazu wäre genau dann hoch, wenn die %TBR sehr gering wäre, Hypoglykämien also kaum oder gar nicht aufgetreten wären.
Aus dem Auftrag der einzelnen, in den zusammengesetzten Metriken ermittelten Werten in den Streudiagrammen, lassen sich die Zusammenhänge grafisch darstellen. Darin zu finden sind die Daten aus den iscCGM-Profilen für den GRI im Vergleich zum Q-Score, den Q-Score im Vergleich zum PGR des Glukosepentagons und des GRI im Vergleich zum PGR des Glukosepentagons jeweils von MmT1D und MmT2D (Abbildung 3).
Aus den sich aus dem Vergleich der Daten in den einzelnen zusammengesetzten Metriken ergebenden Umrechnungsbeziehungen folgt eine Umrechnungsmatrix für den Q-Score mit anderen Parametern der glykämischen Kontrolle (Tabelle 3). Die Werte basieren auf Regressionen des Q-Scores mit TIR, GMI, GRI und CGP und wurden aus berechneten Regressionslinien für MmT1D und MmT2D ausgelesen. Entsprechend Abbildung 3 liegen die Unterschiede zwischen beiden Diabetestypen im Bereich der Messtoleranz von CGM-Sytemen (also einer mittleren absoluten relativen Differenz (MARD) von ≤ 10 % [Kovatchev 2015]), so dass die Werte in der Umrechnungsmatrix von Tabelle 3 für beide Diabetestypen anwendbar sind.
Zusammenfassung
Belegt durch die großen wegweisenden Studien DCCT und UKPDS ergab sich, dass der HbA1c-Wert als Parameter für das Risiko der Entwicklung von DFE etabliert wurde. Mit der Verbreitung von CGM etablierten sich verschiedene Größen wie die %TIR, %TAR, %TBR oder der GMI aus der Analyse von CGM-Daten. Diese sind geeignet, um die gemessene Glykämie zu beschreiben. Weniger gut geeignet sind sie, um das Risiko für die Entwicklung von DFE abzuschätzen, zumindest nicht als einzelne Parameter. Dazu bedürfte es des HbA1c-Wertes, der aber durch verschiedene Einflussfaktoren, z. B. eine Hämolyse verfälscht sein kann [Fath 2016]. Erwünscht ist aber, aufgrund der durch das CGM ermittelten Daten, unmittelbar auf das Risiko für DFE schließen zu können, ohne die zusätzliche Messung des HbA1c. In der Folge wurde z. B. versucht die %TIR mit gleichzeitig vorliegenden HbA1c-Werten zu korrelieren [Vigersky 2019], um aus CGM-Daten allein Aussagen über das Risiko von DFE zu erhalten, was aber nicht zu befriedigenden Ergebnissen führte.
Ausgangspunkt der vorgestellten Analyse war die Überlegung, durch Verwendung einer aus CGM-Daten abgeleiteten zusammengesetzten Metrik das Risiko für die Entwicklung von DFE mit einem einzelnen Wert darzustellen. Dieser Wert sollte eine vergleichbare Bedeutung haben wie der HbA1c, allerdings erweitert um wesentliche glykämische Parameter.
Der Q-Score weist lineare Korrelationen mit dem GMI (r = 0,882) und dem GRI (r = 0,931), sowie eine logarithmische Korrelation mit dem PGR des Glukosepentagons (r = 0,930) auf (Tabelle 3, Abbildungen 3B und 3C). Der PGR des Glukosepentagons hatte eine logarithmische Beziehung zum GRI (r = 0,963), zum Q-Score (r = 0,930) und zum GRI (Tabelle 2, Abbildungen 3B, 3C). Basierend auf diesen Relationen lassen sich entsprechend Tabelle 3 bzw. mit den sich aus den Regressionsrechnungen ergebenden mathematischen Beziehungen die Werte für die anderen Metriken ermitteln.
Die drei zusammengesetzten Metriken Q-Score, Glukosepentagon und GRI nutzen unterschiedliche Parameter aus der CGM-Messung. Sie weisen eine größere Nähe zur bestehenden glykämischen Kontrolle von MmD auf als der HbA1c, der GMI oder die %TIR allein oder auch in Kombination von HbA1c oder GMI mit der %TIR. Wie erwünscht wird die Komplexität der zusammengesetzten Metriken in nur einem einzigen relevanten Parameter zusammengefasst, welcher aber auch hypo- und hyperglykämische Werte und die Glukosevariabilität enthält. Dieser eine, sich aus den Metriken ergebende Parameter dürfte für das diabetologische Fachpersonal auch unter Alltagsbedingungen einfach und schnell zu überblicken sein. Die gute Korrelation der anhand von DFE validierten Metrik des Glukosepentagons mit dem HbA1c belegen, dass diese Validierung eine hohe Relevanz besitzt. Die beiden anderen zusammengesetzten Metriken, der Q-Score und der GRI, haben durch ihre gute Korrelation mit dem Glukosepentagon und der Möglichkeit in dessen Daten umgerechnet zu werden, die gleiche Relevanz. Zusätzlich gewährleisten die Bilder in dem Glukosepentagon einen unmittelbaren Blick auf die Glukosestoffwechselsituation und zeigen im Falle von Stoffwechseloptierungen visuell den Erfolg (siehe Abbildung 2). Bemerkenswert ist, dass funktionelle mathematische Beziehungen die Umrechnung zwischen den drei zusammengesetzten Metriken ermöglichen, obwohl verschiedene Parameter in diesen Metriken genutzt werden. Das bestätigt, dass die Vielzahl der glykämischen Größen miteinander im Zusammenhang stehen. Deshalb sind zusammengesetzte Metriken für eine umfassende Beurteilung des Risikos der Entwicklung von DFE notwendig. Die Korrelation von Einzelwerten mit dem ebenfalls Limitierungen aufweisenden HbA1c ist da unzureichend.
Als limitierend erweist sich, dass aktuell die Metriken nicht in der Software der CGM-Hersteller ausgewiesen werden. Dies ist lediglich der Fall für das Glukosepentagon im "Nightscout Reporter". Ohne eine Übernahme der Berechnungen in die Herstellersoftware werden die dargestellten Zusammenhänge – und damit die Verifizierung eines Qualitätsparameters für die Stoffwechseleinstellung in Bezug auf das Risiko für die Entwicklung von DFE – allein aus CGM-Daten nicht zur Anwendung kommen.
Eine grundsätzliche Limitierung ist vermutlich nicht aufzuheben, nämlich die Parameter der zusammengesetzten Metriken so zu validieren, wie dies beim HbA1c erfolgt ist. Das bedürfte einer Studie wie der DCCT, durchgeführt mit CGM über einen längeren Zeitraum. Aus finanzieller Sicht erscheint dies aktuell nicht möglich.
|
|
Erschienen in: Diabetes, Stoffwechsel und Herz, 2026; 35 (1) Seite 9-18


